Janumet voor de behandeling van diabetes
Merknaam: Janumet
Generieke naam: Sitagliptine en metforminehydrochloride
Inhoud:
Aanwijzingen en gebruik
Dosering en administratie
Doseringsvormen en sterktes
Contra
Waarschuwingen en voorzorgsmaatregelen
Bijwerkingen
Geneesmiddelinteracties
Gebruik in specifieke populaties
Overdose
Beschrijving
farmacologie
Niet-klinische Toxicologie
Klinische studies
Hoe geleverd
Informatie voor patiëntbegeleiding
Janumet, Sitagliptin en Metformin Hydrochloride, Patiëntinformatie (In gewoon Engels)
WAARSCHUWING: LACTISCHE ACIDOSE
Lactaatacidose is een zeldzame, maar ernstige complicatie die kan optreden als gevolg van accumulatie van metformine. Het risico neemt toe met aandoeningen zoals sepsis, uitdroging, overmatig alcoholgebruik, leverinsufficiëntie, nierinsufficiëntie en acuut congestief hartfalen.
Het begin is vaak subtiel en gaat alleen gepaard met niet-specifieke symptomen zoals malaise, myalgie, ademnood, toenemende slaperigheid en niet-specifieke buikpijn. Afwijkingen in het laboratorium zijn lage pH, verhoogde anion gap en verhoogde lactaat in het bloed.
Als acidose wordt vermoed, Janumet1 moet worden stopgezet en moet de patiënt onmiddellijk in het ziekenhuis worden opgenomen. [Zien Waarschuwingen en voorzorgsmaatregelen]
Aanwijzingen en gebruik
Janumet is geïndiceerd als een aanvulling op dieet en lichaamsbeweging om de glykemische controle bij volwassenen met diabetes mellitus type 2 te verbeteren wanneer behandeling met zowel sitagliptine als metformine geschikt is. [Zien Klinische studies.]
Belangrijke gebruiksbeperkingen
Janumet mag niet worden gebruikt bij patiënten met diabetes type 1 of voor de behandeling van diabetische ketoacidose, omdat het in deze situaties niet effectief zou zijn.
Janumet is niet onderzocht in combinatie met insuline.
top
Dosering en administratie
Aanbevolen dosering
De dosering van antihyperglycemische therapie met Janumet moet worden geïndividualiseerd op basis van het huidige regime van de patiënt, effectiviteit en verdraagbaarheid zonder de maximale aanbevolen dagelijkse dosis van 100 mg sitagliptine en 2000 mg te overschrijden metformine. De initiële combinatietherapie of het onderhoud van combinatietherapie moet worden geïndividualiseerd en aan het oordeel van de zorgverlener worden overgelaten.
Janumet moet in het algemeen tweemaal daags bij de maaltijd worden gegeven, met geleidelijke dosisverhoging, om de gastro-intestinale (GI) bijwerkingen als gevolg van metformine te verminderen.
De startdosis van Janumet moet gebaseerd zijn op het huidige regime van de patiënt. Janumet moet tweemaal daags bij de maaltijd worden gegeven. De volgende doses zijn beschikbaar:
50 mg sitagliptine / 500 mg metforminehydrochloride
50 mg sitagliptine / 1000 mg metforminehydrochloride.
Patiënten worden onvoldoende gecontroleerd met alleen voeding en lichaamsbeweging
Als therapie met een combinatietablet die sitagliptine en metformine bevat geschikt wordt geacht voor een patiënt met diabetes mellitus type 2 onvoldoende beheerst met alleen voeding en lichaamsbeweging, de aanbevolen startdosis is tweemaal daags 50 mg sitagliptine / 500 mg metforminehydrochloride dagelijks. Patiënten met onvoldoende glykemische controle van deze dosis kunnen worden getitreerd tot 50 mg sitagliptine / 1000 mg metforminehydrochloride tweemaal daags.
Patiënten onvoldoende gecontroleerd op metformine monotherapie
Als therapie met een combinatietablet die sitagliptine en metformine bevat geschikt wordt geacht voor een patiënt die onvoldoende metformine alleen onder controle wordt gehouden, aanbevolen startdosis Janumet moet sitagliptine bevatten gedoseerd als 50 mg tweemaal daags (100 mg totale dagelijkse dosis) en de dosis metformine is al genomen. Voor patiënten die 850 mg tweemaal daags metformine gebruiken, is de aanbevolen startdosis Janumet tweemaal daags 50 mg sitagliptine / 1000 mg metforminehydrochloride.
Patiënten onvoldoende behandeld met monotherapie met sitagliptine
Als therapie met een combinatietablet die sitagliptine en metformine bevat, onvoldoende wordt geacht voor een patiënt gecontroleerd met alleen sitagliptine, is de aanbevolen startdosis van Janumet 50 mg sitagliptine / 500 mg metforminehydrochloride tweemaal dagelijks. Patiënten met onvoldoende controle op deze dosis kunnen worden getitreerd tot 50 mg sitagliptine / 1000 mg metforminehydrochloride tweemaal daags. Patiënten die sitagliptine monotherapie gebruiken, dosisaangepast voor nierinsufficiëntie, moeten niet worden overgeschakeld naar Janumet [zie Contra].
Patiënten die overschakelen van gelijktijdige toediening van sitagliptine en metformine
Voor patiënten die overschakelen van sitagliptine gelijktijdig toegediend met metformine, kan Janumet worden gestart met de dosis sitagliptine en metformine die al wordt ingenomen.
Patiënten die onvoldoende worden behandeld met dubbele combinatietherapie met twee van de volgende antihyperglycemische middelen: sitagliptine, metformine of een sulfonylureumderivaat
Als therapie met een combinatietablet die sitagliptine en metformine bevat, hierin passend wordt geacht instelling, moet de gebruikelijke startdosis Janumet sitagliptine geven gedoseerd als 50 mg tweemaal daags (100 mg in totaal dagelijkse dosis). Bij het bepalen van de startdosis van de metforminecomponent moet rekening worden gehouden met het niveau van glycemische controle van de patiënt en de huidige dosis (indien aanwezig) metformine. Een geleidelijke dosisverhoging om de gastro-intestinale (GI) bijwerkingen geassocieerd met metformine te verminderen moet worden overwogen. Patiënten die momenteel sulfonylureum gebruiken of starten, kunnen lagere doses sulfonylureum nodig hebben om het risico op hypoglykemie te verminderen [zie Waarschuwingen en voorzorgsmaatregelen].
Er zijn geen onderzoeken uitgevoerd die specifiek de veiligheid en werkzaamheid van Janumet hebben onderzocht bij patiënten die eerder werden behandeld met andere orale antihyperglycemische middelen en die overstapten op Janumet. Elke verandering in de therapie van type 2 diabetes moet met voorzichtigheid en passende monitoring worden uitgevoerd, omdat veranderingen in de glykemische controle kunnen optreden.
top
Doseringsvormen en sterktes
- 50 mg / 500 mg tabletten zijn lichtroze, capsulevormige, filmomhulde tabletten met aan één zijde de inscriptie "575".
- 50 mg / 1000 mg tabletten zijn rode, capsulevormige, filmomhulde tabletten met aan één zijde de inscriptie "577".
top
Contra
Janumet (sitagliptine / metformine HCl) is gecontra-indiceerd bij patiënten met:
- Nierziekte of nierfunctiestoornis, bijvoorbeeld, zoals gesuggereerd door serumcreatininespiegels â ‰ ¥ 1,5 mg / dL [mannen], â ‰ ¥ 1,4 mg / dL [vrouwen] of abnormaal creatinineklaring die ook het gevolg kan zijn van aandoeningen zoals cardiovasculaire collaps (shock), acuut myocardinfarct en septikemie [zien Waarschuwingen en voorzorgsmaatregelen].
- Acute of chronische metabole acidose, inclusief diabetische ketoacidose, met of zonder coma.
- Voorgeschiedenis van een ernstige overgevoeligheidsreactie op Janumet of sitagliptine (een van de componenten van Janumet), zoals anafylaxie of angio-oedeem. [Zien Waarschuwingen en voorzorgsmaatregelen en Bijwerkingen.]
Janumet moet tijdelijk worden stopgezet bij patiënten die radiologische onderzoeken ondergaan waarbij intravasculair is betrokken toediening van gejodeerde contraststoffen, omdat het gebruik van dergelijke producten kan leiden tot een acute nierverandering functie [zie Waarschuwingen en voorzorgsmaatregelen].
top
Waarschuwingen en voorzorgsmaatregelen
Melkzuuracidose
Metformin hydrochloride
Lactaatacidose is een zeldzame, maar ernstige, metabole complicatie die kan optreden als gevolg van accumulatie van metformine tijdens de behandeling met Janumet; wanneer het optreedt, is het dodelijk in ongeveer 50% van de gevallen. Lactaatacidose kan ook optreden in combinatie met een aantal pathofysiologische aandoeningen, waaronder diabetes mellitus, en wanneer er sprake is van significante weefselhypoperfusie en hypoxemie. Lactaatacidose wordt gekenmerkt door verhoogde bloedlactaatspiegels (> 5 mmol / L), verlaagde bloed-pH, elektrolytstoornissen met een verhoogde anion gap en een verhoogde lactaat / pyruvaat-verhouding. Wanneer metformine als oorzaak van melkzuuracidose wordt betrokken, worden in het algemeen metformine-plasmaspiegels> 5 µg / ml gevonden.
De gerapporteerde incidentie van lactaatacidose bij patiënten die metforminehydrochloride krijgen, is zeer laag (ongeveer 0,03 gevallen / 1000 patiëntjaren, met ongeveer 0,015 fatale gevallen / 1000 patiëntjaren). In klinische onderzoeken van meer dan 20.000 patiëntjaren aan metformine waren er geen meldingen van lactaatacidose. Gemelde gevallen zijn voornamelijk opgetreden bij diabetespatiënten met significante nierinsufficiëntie, inclusief beide intrinsieke nier ziekte en renale hypoperfusie, vaak in de context van meerdere gelijktijdige medische / chirurgische problemen en meerdere gelijktijdige medicijnen. Patiënten met congestief hartfalen die farmacologisch beheer vereisen, in het bijzonder patiënten met onstabiel of acuut congestief hartfalen met een risico op hypoperfusie en hypoxemie, hebben een verhoogd risico op melkzuur acidose. Het risico op lactaatacidose neemt toe met de mate van nierdisfunctie en de leeftijd van de patiënt. Het risico op lactaatacidose kan daarom aanzienlijk worden verminderd door regelmatige controle van de nierfunctie bij patiënten die metformine gebruiken en door de minimale effectieve dosis metformine te gebruiken. In het bijzonder moet de behandeling van ouderen gepaard gaan met een zorgvuldige controle van de nierfunctie. Behandeling met metformine dient niet te worden gestart bij patiënten van ≥ 80 jaar oud, tenzij de creatinineklaring wordt gemeten toont aan dat de nierfunctie niet wordt verminderd, omdat deze patiënten gevoeliger zijn voor het ontwikkelen van lactaatacidose. Bovendien moet metformine onmiddellijk worden onthouden in de aanwezigheid van een aandoening geassocieerd met hypoxemie, uitdroging of sepsis. Omdat een verminderde leverfunctie het vermogen om lactaat te zuiveren aanzienlijk kan beperken, moet metformine in het algemeen worden vermeden bij patiënten met klinische of laboratoriumgegevens van leveraandoeningen. Patiënten moeten worden gewaarschuwd tegen overmatige inname van alcohol, hetzij acuut of chronisch, wanneer ze metformine gebruiken, omdat alcohol de effecten van metforminehydrochloride op het lactaatmetabolisme versterkt. Bovendien moet metformine tijdelijk worden stopgezet voorafgaand aan een intravasculair radiocontrastonderzoek en voor elke chirurgische procedure [zie Waarschuwingen en voorzorgsmaatregelen].
Het begin van lactaatacidose is vaak subtiel en gaat alleen gepaard met niet-specifieke symptomen zoals malaise, myalgie, ademnood, toenemende slaperigheid en niet-specifieke buikpijn. Er kunnen hypothermie, hypotensie en resistente bradyaritmieën geassocieerd zijn met duidelijkere acidose. De patiënt en de arts van de patiënt moeten zich bewust zijn van het mogelijke belang van dergelijke symptomen en de patiënt moet de instructie krijgen om de arts onmiddellijk op de hoogte te stellen als ze optreden [zie Waarschuwingen en voorzorgsmaatregelen]. Metformine moet worden ingetrokken totdat de situatie is opgehelderd. Serumelektrolyten, ketonen, bloedglucose en, indien aangegeven, bloed-pH, lactaatniveaus en zelfs bloedmetforminespiegels kunnen nuttig zijn. Als een patiënt eenmaal is gestabiliseerd op een dosisniveau van metformine, is het onwaarschijnlijk dat gastro-intestinale symptomen, die vaak optreden tijdens het begin van de therapie, verband houden met het geneesmiddel. Later optreden van gastro-intestinale symptomen kan te wijten zijn aan lactaatacidose of een andere ernstige ziekte.
Niveaus van nuchtere veneuze plasmalactaat boven de bovengrens van normaal, maar minder dan 5 mmol / L bij patiënten die metformine gebruiken, duiden niet noodzakelijk op dreigend melkzuur acidose en kan verklaard worden door andere mechanismen, zoals slecht gereguleerde diabetes of obesitas, krachtige fysieke activiteit of technische problemen bij het hanteren van monsters [zien Waarschuwingen en voorzorgsmaatregelen].
Lactaatacidose moet worden vermoed bij elke diabetespatiënt met metabole acidose zonder bewijs van ketoacidose (ketonurie en ketonemie).
Lactaatacidose is een medisch noodgeval dat in een ziekenhuisomgeving moet worden behandeld. Bij een patiënt met lactaatacidose die metformine gebruikt, moet het medicijn onmiddellijk worden gestaakt en moeten onmiddellijk algemene ondersteunende maatregelen worden genomen. Omdat metforminehydrochloride dialyseerbaar is (met een klaring tot 170 ml / min bij goede hemodynamische eigenschappen) omstandigheden), wordt snelle hemodialyse aanbevolen om de acidose te corrigeren en de opgehoopte te verwijderen metformine. Dergelijk beheer resulteert vaak in een snelle omkering van symptomen en herstel [zie Contra; Waarschuwingen en voorzorgsmaatregelen].
Verminderde leverfunctie
Aangezien een verminderde leverfunctie is geassocieerd met sommige gevallen van lactaatacidose, moet Janumet in het algemeen worden vermeden bij patiënten met klinische of laboratoriumgegevens van leveraandoeningen.
Beoordeling van de nierfunctie
Van metformine en sitagliptine is bekend dat ze substantieel door de nier worden uitgescheiden. Het risico op accumulatie van metformine en lactaatacidose neemt toe met de mate van nierinsufficiëntie. Patiënten met serumcreatininespiegels boven de normale bovengrens voor hun leeftijd mogen daarom geen Janumet krijgen. Bij ouderen moet Janumet zorgvuldig worden getitreerd om de minimumdosis voor een adequaat glycemisch effect vast te stellen, omdat veroudering kan worden geassocieerd met een verminderde nierfunctie. [Zien Waarschuwingen en voorzorgsmaatregelen en Gebruik in specifieke populaties.]
Voor aanvang van de behandeling met Janumet en minimaal jaarlijks daarna moet de nierfunctie worden beoordeeld en geverifieerd als normaal. Bij patiënten bij wie de ontwikkeling van nierdisfunctie wordt verwacht, met name bij oudere patiënten, nier functie moet vaker worden beoordeeld en Janumet stopgezet als er aanwijzingen zijn voor nierinsufficiëntie Cadeau.
Vitamine B12 levels
In gecontroleerde klinische onderzoeken met metformine van 29 weken, een afname tot subnormale niveaus van voorheen normaal serum Vitamine B12 niveaus, zonder klinische manifestaties, werden waargenomen bij ongeveer 7% van de patiënten. Een dergelijke afname, mogelijk als gevolg van interferentie met B12 absorptie uit de B12-intrinsieke factorcomplex, is echter zeer zelden geassocieerd met bloedarmoede en lijkt snel omkeerbaar te zijn bij stopzetting van metformine of vitamine B12 aanvulling. Het meten van hematologische parameters op jaarbasis wordt geadviseerd bij patiënten op Janumet en alle zichtbare afwijkingen moeten naar behoren worden onderzocht en beheerd. [Zien Bijwerkingen.]
Bepaalde personen (personen met onvoldoende vitamine B12 of calciuminname of -absorptie) lijken vatbaar te zijn voor het ontwikkelen van subnormale vitamine B12 levels. Bij deze patiënten, routine serum Vitamine B12 metingen met tussenpozen van twee tot drie jaar kunnen nuttig zijn.
Alcoholinname
Het is bekend dat alcohol het effect van metformine op het lactaatmetabolisme versterkt. Patiënten moeten daarom worden gewaarschuwd voor overmatige alcoholinname, acuut of chronisch, tijdens het gebruik van Janumet.
Chirurgische procedures
Het gebruik van Janumet moet tijdelijk worden opgeschort voor elke chirurgische procedure (behalve kleine procedures die niet gepaard gaan met een beperkte inname van voedsel en vloeistoffen) en mag niet opnieuw worden gestart totdat de orale inname van de patiënt is hervat en de nierfunctie is geëvalueerd als normaal.
Verandering in klinische status van patiënten met eerder gecontroleerde diabetes type 2
Een patiënt met diabetes type 2 die voorheen goed onder controle was van Janumet en die laboratoriumafwijkingen of klinische afwijkingen ontwikkelt ziekte (vooral vage en slecht gedefinieerde ziekte) moet onmiddellijk worden geëvalueerd op tekenen van ketoacidose of melkzuur acidose. Evaluatie moet serumelektrolyten en ketonen, bloedglucose en, indien aangegeven, bloed-pH, lactaat, pyruvaat en metforminewaarden omvatten. Als acidose van beide vormen optreedt, moet Janumet onmiddellijk worden gestopt en moeten andere passende corrigerende maatregelen worden genomen.
Gebruik met medicijnen waarvan bekend is dat ze hypoglykemie kunnen veroorzaken
sitagliptine
Zoals typisch is voor andere antihyperglycemische middelen die worden gebruikt in combinatie met een sulfonylureum, wanneer sitagliptine werd gebruikt in combinatie met metformine en een sulfonylureum, een medicijn waarvan bekend is dat het hypoglykemie veroorzaakt, de incidentie van hypoglykemie was hoger dan die van placebo in combinatie met metformine en een sulfonylureum [zie Bijwerkingen]. Daarom kunnen patiënten die ook een insulinesecretagoog ontvangen (bijvoorbeeld sulfonylureum, meglitinide) een lagere dosis van de insulinesecretagoog nodig hebben om het risico op hypoglykemie te verminderen [zie Dosering en administratie].
Metformin hydrochloride
Hypoglykemie treedt niet op bij patiënten die alleen metformine krijgen onder gebruikelijke gebruiksomstandigheden, maar kan optreden wanneer de calorie-inname onvoldoende is, wanneer zware inspanning wordt niet gecompenseerd door calorische suppletie of tijdens gelijktijdig gebruik met andere glucoseverlagende middelen (zoals sulfonylureumderivaten en insuline) of ethanol. Oudere, verzwakte of ondervoede patiënten en patiënten met bijnier- of hypofyse-insufficiëntie of alcoholintoxicatie zijn bijzonder gevoelig voor hypoglycemische effecten. Hypoglykemie kan moeilijk te herkennen zijn bij ouderen en bij mensen die β-adrenerge blokkerende geneesmiddelen gebruiken.
Gelijktijdige medicijnen die de nierfunctie of metformine beïnvloeden
Gelijktijdige medicatie (s) die de nierfunctie kunnen beïnvloeden of kunnen leiden tot significante hemodynamische verandering of kunnen interfereren met de dispositie van metformine, zoals kationische geneesmiddelen die worden geëlimineerd door renale tubulaire secretie [zien Geneesmiddelinteracties], moet met voorzichtigheid worden gebruikt.
Radiologische studies met intravasculaire gejodeerde contrastmaterialen
Intravasculaire contraststudies met gejodeerde materialen (bijvoorbeeld intraveneuze urogram, intraveneuze cholangiografie, angiografie en computertomografie (CT) scans met intravasculaire contrastmaterialen) kan leiden tot acute verandering van de nierfunctie en zijn in verband gebracht met lactaatacidose bij patiënten die metformine krijgen [zie Contra]. Daarom moet Janumet bij patiënten bij wie een dergelijk onderzoek is gepland, tijdelijk worden stopgezet op het moment van of voorafgaand aan de procedure, en 48 uur na de procedure onthouden en alleen hersteld nadat de nierfunctie opnieuw is geëvalueerd en is vastgesteld dat normaal zijn.
Hypoxische staten
Cardiovasculaire collaps (shock) door welke oorzaak dan ook, acuut congestief hartfalen, acuut myocardinfarct en andere aandoeningen gekenmerkt door hypoxemie zijn in verband gebracht met lactaatacidose en kunnen ook prerenaal veroorzaken azotemie. Wanneer dergelijke voorvallen optreden bij patiënten die met Janumet worden behandeld, moet het medicijn onmiddellijk worden stopgezet.
Verlies van controle over bloedglucose
Wanneer een patiënt gestabiliseerd op een diabetisch regime wordt blootgesteld aan stress zoals koorts, trauma, infectie of chirurgie, kan een tijdelijk verlies van glycemische controle optreden. Op dergelijke momenten kan het nodig zijn om Janumet in te houden en tijdelijk insuline toe te dienen. Janumet kan worden hersteld nadat de acute episode is opgelost.
Overgevoeligheidsreacties
Er zijn postmarketingmeldingen geweest van ernstige overgevoeligheidsreacties bij patiënten die werden behandeld met sitagliptine, een van de componenten van Janumet. Deze reacties omvatten anafylaxie, angio-oedeem en exfoliatieve huidaandoeningen, waaronder het syndroom van Stevens-Johnson. Omdat deze reacties vrijwillig worden gemeld door een populatie van onzekere omvang, is dat over het algemeen het geval niet mogelijk om hun frequentie betrouwbaar te schatten of een oorzakelijk verband te leggen met de blootstelling aan geneesmiddelen. Het optreden van deze reacties trad op binnen de eerste 3 maanden na het begin van de behandeling met sitagliptine, met enkele meldingen na de eerste dosis. Als een overgevoeligheidsreactie wordt vermoed, stop dan met Janumet, onderzoek naar andere mogelijke oorzaken voor het evenement en stel een alternatieve behandeling voor diabetes in. [Zien Bijwerkingen.]
Macrovasculaire resultaten
Er zijn geen klinische onderzoeken geweest die overtuigend bewijs van macrovasculaire risicovermindering met Janumet of enig ander antidiabetisch geneesmiddel hebben aangetoond.
top
Bijwerkingen
Klinische proeven Ervaring
Omdat klinische onderzoeken onder sterk uiteenlopende omstandigheden worden uitgevoerd, zijn bijwerkingen waargenomen in de klinische onderzoeken van een geneesmiddel kan niet direct worden vergeleken met de tarieven in de klinische proeven met een ander geneesmiddel en is mogelijk geen afspiegeling van de waargenomen waarden in praktijk.
Sitagliptine en metformine Gelijktijdige toediening bij patiënten met diabetes type 2 onvoldoende gecontroleerd op dieet en lichaamsbeweging
Tabel 1 geeft een overzicht van de meest voorkomende (â ‰ ¥ 5% van de patiënten) gemelde bijwerkingen (ongeacht de door de onderzoeker vastgestelde causaliteit) placebogecontroleerd factoronderzoek waarin sitagliptine en metformine gelijktijdig werden toegediend aan patiënten met diabetes type 2 die onvoldoende werden gecontroleerd op dieet en oefening.
Tabel 1: Sitagliptine en metformine Gelijktijdig toegediend aan patiënten met diabetes type 2 onvoldoende gecontroleerd op dieet en lichaamsbeweging: bijwerkingen Gemeld (ongeacht de onderzoeker van de causaliteit) bij â ‰ ¥ 5% van de patiënten die combinatietherapie ontvangen (en groter dan bij patiënten die ontvangen worden Placebo)*
| Aantal patiënten (%) | ||||
Placebo |
sitagliptine 100 mg QD |
Metformine 500 mg / Metformine 1000 mg bid†|
sitagliptine 50 mg bid + Metformine 500 mg / Metformine 1000 mg bid†|
|
| N = 176 | N = 179 | N = 364†| N = 372†| |
| ||||
| Diarree | 7 (4.0) | 5 (2.8) | 28 (7.7) | 28 (7.5) |
| Bovenste luchtwegeninfectie | 9 (5.1) | 8 (4.5) | 19 (5.2) | 23 (6.2) |
| Hoofdpijn | 5 (2.8) | 2 (1.1) | 14 (3.8) | 22 (5.9) |
Sitagliptine add-on therapie bij patiënten met diabetes type 2 Onvoldoende gecontroleerd met alleen metformine
In een placebogecontroleerd onderzoek van 24 weken sitagliptine 100 mg eenmaal daags toegediend toegevoegd aan een tweemaal daags metformine-regime waren er geen bijwerkingen gemeld ongeacht de beoordeling door de onderzoeker van het oorzakelijk verband bij â ‰ ¥ 5% van de patiënten en vaker dan bij gegeven patiënten placebo. Staken van de behandeling vanwege klinische bijwerkingen was vergelijkbaar met de placebogroep (sitagliptine en metformine, 1,9%; placebo en metformine, 2,5%).
hypoglykemie
Bijwerkingen van hypoglykemie waren gebaseerd op alle meldingen van hypoglykemie; een gelijktijdige glucosemeting was niet vereist. De algehele incidentie van vooraf gespecificeerde bijwerkingen van hypoglykemie bij patiënten met diabetes type 2 die onvoldoende werden gecontroleerd op dieet en lichaamsbeweging, was patiënten die placebo kregen, 0,6% bij patiënten die alleen sitagliptine kregen, 0,8% bij patiënten die alleen metformine kregen en 1,6% bij patiënten die sitagliptine kregen in combinatie met metformine. Bij patiënten met diabetes type 2 die onvoldoende worden gereguleerd met alleen metformine, is de algemene incidentie van bijwerkingen reacties van hypoglykemie was 1,3% bij patiënten die add-on sitagliptine kregen en 2,1% bij patiënten die add-on kregen placebo.
Gastro-intestinale bijwerkingen
De incidentie van vooraf geselecteerde gastro-intestinale bijwerkingen bij patiënten behandeld met sitagliptine en metformine waren vergelijkbaar met die gemeld voor patiënten die alleen met metformine werden behandeld. Zie tabel 2.
Tabel 2: Voorgeselecteerde gastro-intestinale bijwerkingen (ongeacht de onderzoeker van de causaliteit) gerapporteerd bij patiënten met diabetes type 2 die sitagliptine en metformine kregen.
| Aantal patiënten (%) | ||||||
| Studie van sitagliptine en metformine bij patiënten die onvoldoende onder controle zijn op dieet en lichaamsbeweging |
Studie van Sitagliptin-add-on bij patiënten die onvoldoende met alleen metformine werden gecontroleerd | |||||
Placebo |
sitagliptine 100 mg QD |
Metformine 500 mg / Metformine 1000 mg bid* |
sitagliptine 50 mg bid + Metformine 500 mg / Metformine 1000 mg bid* |
Placebo en metformine â ‰ ¥ 1500 mg per dag |
Sitagliptin 100 mg QD en Metformin â ‰ ¥ 1500 mg per dag |
|
| N = 176 | N = 179 | N = 364 | N = 372 | N = 237 | N = 464 | |
| ||||||
| Diarree | 7 (4.0) | 5 (2.8) | 28 (7.7) | 28 (7.5) | 6 (2.5) | 11 (2.4) |
| Misselijkheid | 2 (1.1) | 2 (1.1) | 20 (5.5) | 18 (4.8) | 2 (0.8) | 6 (1.3) |
| braken | 1 (0.6) | 0 (0.0) | 2 (0.5) | 8 (2.2) | 2 (0.8) | 5 (1.1) |
| Buikpijn†| 4 (2.3) | 6 (3.4) | 14 (3.8) | 11 (3.0) | 9 (3.8) | 10 (2.2) |
Sitagliptine in combinatie met Metformine en Glimepiride
In een 24-weken durende placebogecontroleerde studie van sitagliptine 100 mg als aanvullende therapie bij patiënten met diabetes type 2 onvoldoende gecontroleerd op metformine en glimepiride (sitagliptine, N = 116; placebo, N = 113), de gerapporteerde bijwerkingen, ongeacht de beoordeling door de onderzoeker van het oorzakelijk verband bij â ‰ ¥ 5% van de patiënten behandeld met sitagliptine en vaker dan bij patiënten behandeld met placebo waren: hypoglykemie (sitagliptine, 16,4%; placebo, 0,9%) en hoofdpijn (6,9%, 2,7%).
Er werden geen klinisch betekenisvolle veranderingen in vitale functies of in ECG (inclusief in QTc-interval) waargenomen met de combinatie van sitagliptine en metformine.
De meest voorkomende bijwerkingen bij monotherapie met sitagliptine zijn gemeld ongeacht de onderzoeker beoordeling van causaliteit bij â ‰ ¥ 5% van de patiënten en vaker dan bij patiënten die placebo kregen nasofaryngitis.
De meest voorkomende (> 5%) vastgestelde bijwerkingen als gevolg van het starten van metformine-therapie zijn diarree, misselijkheid / braken, winderigheid, buikpijn, indigestie, asthenie en hoofdpijn.
Laboratorium testen
sitagliptine
De incidentie van laboratoriumbijwerkingen was vergelijkbaar bij patiënten die werden behandeld met sitagliptine en metformine (7,6%) in vergelijking met patiënten die werden behandeld met placebo en metformine (8,7%). In de meeste, maar niet alle studies, een kleine toename van het aantal witte bloedcellen (ongeveer 200 cellen / microL verschil in WBC versus placebo; gemiddelde baseline WBC ongeveer 6600 cellen / microL) werd waargenomen vanwege een kleine toename in neutrofielen. Deze verandering in laboratoriumparameters wordt niet als klinisch relevant beschouwd.
Metformin hydrochloride
In gecontroleerde klinische onderzoeken met metformine van 29 weken, een afname tot subnormale niveaus van voorheen normaal serum Vitamine B12 niveaus, zonder klinische manifestaties, werden waargenomen bij ongeveer 7% van de patiënten. Een dergelijke afname, mogelijk als gevolg van interferentie met B12 absorptie uit de B12-intrinsieke factorcomplex, is echter zeer zelden geassocieerd met bloedarmoede en lijkt snel omkeerbaar te zijn bij stopzetting van metformine of vitamine B12 aanvulling. [Zien Waarschuwingen en voorzorgsmaatregelen.]
Postmarketing ervaring
De volgende aanvullende bijwerkingen zijn vastgesteld tijdens het gebruik van Janumet of sitagliptine, een van de componenten van Janumet na goedkeuring. Omdat deze reacties vrijwillig worden gemeld door een populatie van onzekere omvang, is dat over het algemeen het geval niet mogelijk om hun frequentie betrouwbaar te schatten of een oorzakelijk verband te leggen met de blootstelling aan geneesmiddelen.
Overgevoeligheidsreacties omvatten anafylaxie, angio-oedeem, huiduitslag, urticaria, cutane vasculitis en exfoliatieve huidaandoeningen waaronder het Stevens-Johnson-syndroom [zie Waarschuwingen en voorzorgsmaatregelen]; bovenste luchtweginfectie; leverenzymverhogingen; pancreatitis.
top
Geneesmiddelinteracties
Kationische medicijnen
Kationische geneesmiddelen (bijv. Amiloride, digoxine, morfine, procaïnamide, kinidine, kinine, ranitidine, triamtereen, trimethoprim of vancomycine) die geëlimineerd door renale tubulaire secretie hebben theoretisch het potentieel voor interactie met metformine door te concurreren voor gemeenschappelijk niertubulair transport systemen. Een dergelijke interactie tussen metformine en oraal cimetidine is waargenomen bij normale gezonde vrijwilligers bij metformine-cimetidine met enkelvoudige en meervoudige doses geneesmiddelinteractiestudies, met een toename van 60% in piekmetformine-plasma en volbloedconcentraties en een 40% toename in plasma en volbloed-metformine AUC. Er was geen verandering in de eliminatiehalfwaardetijd in het onderzoek met enkele dosis. Metformine had geen effect op de farmacokinetiek van cimetidine. Hoewel dergelijke interacties theoretisch blijven (behalve cimetidine), moeten zorgvuldige patiëntbewaking en dosisaanpassing van Janumet en / of de interfererend medicijn wordt aanbevolen bij patiënten die kationische medicijnen gebruiken die worden uitgescheiden via de proximale renale tubulaire secretie systeem.
digoxine
Er was een lichte toename in het gebied onder de curve (AUC, 11%) en gemiddelde piekgeneesmiddelconcentratie (Cmax, 18%) digoxine met gelijktijdige toediening van 100 mg sitagliptine gedurende 10 dagen. Deze verhogingen worden niet waarschijnlijk geacht klinisch zinvol te zijn. Digoxine, als een kationisch medicijn, heeft het potentieel om te concurreren met metformine voor gangbare niertransportsystemen, waardoor de serumconcentraties van ofwel digoxine, metformine of beide worden beïnvloed. Patiënten die digoxine krijgen, moeten op passende wijze worden gecontroleerd. Er wordt geen dosisaanpassing van digoxine of Janumet aanbevolen.
glyburide
In een interactiestudie met één dosis bij type 2 diabetespatiënten resulteerde gelijktijdige toediening van metformine en glyburide niet in veranderingen in de farmacokinetiek van metformine of de farmacodynamiek. Verlaging van de AUC en C van glyburidemax werden waargenomen, maar waren zeer variabel. Het enkele dosis karakter van deze studie en het gebrek aan correlatie tussen glyburide bloedspiegels en farmacodynamische effecten maken de klinische betekenis van deze interactie onzeker.
furosemide
Een onderzoek naar de interactie van metformine-furosemide geneesmiddelen bij een enkele dosis bij gezonde proefpersonen toonde aan dat de farmacokinetische parameters van beide verbindingen werden beïnvloed door gelijktijdige toediening. Furosemide verhoogde het metformine-plasma en bloed Cmax met 22% en bloed-AUC met 15%, zonder enige significante verandering in de nierklaring van metformine. Bij toediening met metformine, de Cmax en AUC van furosemide waren respectievelijk 31% en 12% kleiner dan wanneer alleen toegediend, en de de terminale halfwaardetijd was met 32% verminderd, zonder enige significante verandering in de furosemide-nier klaring. Er is geen informatie beschikbaar over de interactie van metformine en furosemide bij chronische toediening.
nifedipine
Een met-dosis, metformine-nifedipine geneesmiddelinteractie-onderzoek bij normale gezonde vrijwilligers toonde aan dat gelijktijdige toediening van nifedipine de plasmametformine C verhoogdemax en AUC met respectievelijk 20% en 9%, en verhoogde de hoeveelheid uitgescheiden in de urine. Tmax en halfwaardetijd werden niet aangetast. Nifedipine lijkt de absorptie van metformine te verbeteren. Metformine had minimale effecten op nifedipine.
Het gebruik van metformine met andere geneesmiddelen
Bepaalde geneesmiddelen hebben de neiging hyperglykemie te veroorzaken en kunnen leiden tot verlies van glykemische controle. Deze geneesmiddelen omvatten de thiaziden en andere diuretica, corticosteroïden, fenothiazines, schildklierproducten, oestrogenen, orale anticonceptiva, fenytoïne, nicotinezuur, sympathomimetica, calciumantagonisten, en isoniazide. Wanneer dergelijke geneesmiddelen worden toegediend aan een patiënt die Janumet krijgt, moet de patiënt nauwlettend worden geobserveerd om voldoende glykemische controle te behouden.
Bij gezonde vrijwilligers werd de farmacokinetiek van metformine en propranolol en metformine en ibuprofen niet beïnvloed bij gelijktijdige toediening in interactiestudies met één dosis.
Metformine is verwaarloosbaar gebonden aan plasmaproteïnen en heeft daarom minder kans om te interageren met sterk eiwitgebonden medicijnen zoals salicylaten, sulfonamiden, chlooramfenicol en probenecide, in vergelijking met de sulfonylureumderivaten, die uitgebreid zijn gebonden aan serum eiwitten.
top
Gebruik in specifieke populaties
Zwangerschap
Zwangerschap Categorie B:
Janumet
Er zijn geen adequate en goed gecontroleerde onderzoeken bij zwangere vrouwen met Janumet of de afzonderlijke componenten; daarom is de veiligheid van Janumet bij zwangere vrouwen niet bekend. Janumet mag alleen tijdens de zwangerschap worden gebruikt als dit duidelijk nodig is.
Merck & Co., Inc. houdt een register bij om de zwangerschapsresultaten bij te houden van vrouwen die tijdens de zwangerschap aan Janumet zijn blootgesteld. Zorgverleners worden aangemoedigd om elke prenatale blootstelling aan Janumet te melden door de zwangerschapsregistratie te bellen op (800) 986-8999.
Er zijn geen dierstudies uitgevoerd met de gecombineerde producten in Janumet om de effecten op de voortplanting te evalueren. De volgende gegevens zijn gebaseerd op bevindingen in onderzoeken uitgevoerd met sitagliptine of metformine afzonderlijk.
sitagliptine
Er zijn reproductiestudies uitgevoerd bij ratten en konijnen. Doses sitagliptine tot 125 mg / kg (ongeveer 12 keer de blootstelling van de mens bij de maximale aanbevolen dosis voor mensen) hadden geen invloed op de vruchtbaarheid of de foetus. Er zijn echter geen adequate en goed gecontroleerde onderzoeken met sitagliptine bij zwangere vrouwen.
Sitagliptine toegediend aan zwangere vrouwelijke ratten en konijnen vanaf de zwangerschap van dag 6 tot 20 (organogenese) was niet teratogeen bij orale doses tot 250 mg / kg (ratten) en 125 mg / kg (konijnen), of ongeveer 30 en 20 keer menselijke blootstelling bij de maximale aanbevolen dosis voor mensen (MRHD) van 100 mg / dag op basis van de AUC vergelijkingen. Hogere doses verhoogden de incidentie van ribmisvormingen bij nakomelingen met 1000 mg / kg, of ongeveer 100 keer menselijke blootstelling bij de MRHD.
Sitagliptine toegediend aan vrouwelijke ratten vanaf dracht 6 tot lactatiedag 21 verminderde het lichaamsgewicht bij mannelijke en vrouwelijke nakomelingen met 1000 mg / kg. Er werd geen functionele of gedragstoxiciteit waargenomen bij nakomelingen van ratten.
Placentale overdracht van sitagliptine toegediend aan zwangere ratten was ongeveer 45% na 2 uur en 80% na 24 uur na de dosis. Placentale overdracht van sitagliptine toegediend aan zwangere konijnen was ongeveer 66% na 2 uur en 30% na 24 uur.
Metformin hydrochloride
Metformine was niet teratogeen bij ratten en konijnen in doses tot 600 mg / kg / dag. Dit vertegenwoordigt een blootstelling van ongeveer 2 en 6 keer de maximale aanbevolen menselijke dagelijkse dosis van 2000 mg op basis van vergelijkingen van het lichaamsoppervlak voor respectievelijk ratten en konijnen. Bepaling van foetale concentraties toonde een gedeeltelijke placentabarrière voor metformine.
Moeders die borstvoeding geven
Er zijn geen studies uitgevoerd bij lacterende dieren met de gecombineerde componenten van Janumet. In onderzoeken uitgevoerd met de afzonderlijke componenten worden sitagliptine en metformine uitgescheiden in de melk van zogende ratten. Het is niet bekend of sitagliptine wordt uitgescheiden in moedermelk. Omdat veel geneesmiddelen in moedermelk worden uitgescheiden, is voorzichtigheid geboden wanneer Janumet wordt toegediend aan een vrouw die borstvoeding geeft.
Gebruik bij kinderen
De veiligheid en effectiviteit van Janumet bij pediatrische patiënten jonger dan 18 jaar zijn niet vastgesteld.
Geriatrisch gebruik
Janumet
Omdat sitagliptine en metformine substantieel door de nier worden uitgescheiden en omdat veroudering kan worden geassocieerd met een verminderde nierfunctie, moet Janumet met voorzichtigheid worden gebruikt naarmate de leeftijd toeneemt. Voorzichtigheid is geboden bij de dosiskeuze en moet gebaseerd zijn op zorgvuldige en regelmatige controle van de nierfunctie. [Zien Waarschuwingen en voorzorgsmaatregelen; Klinische Farmacologie.]
sitagliptine
Van het totale aantal proefpersonen (N = 3884) in fase II en III klinische onderzoeken met sitagliptine, waren 725 patiënten 65 jaar en ouder, terwijl 61 patiënten 75 jaar en ouder waren. Er werden geen algemene verschillen in veiligheid of effectiviteit waargenomen tussen personen van 65 jaar en ouder en jongere personen. Hoewel deze en andere gerapporteerde klinische ervaringen geen verschillen in respons hebben geïdentificeerd tussen oudere en jongere patiënten kan een grotere gevoeligheid van sommige oudere personen niet zijn uitgesloten.
Metformin hydrochloride
Gecontroleerde klinische studies met metformine omvatten niet voldoende aantallen oudere patiënten om te bepalen of zij anders reageren van jongere patiënten, hoewel andere gerapporteerde klinische ervaring geen verschillen in respons tussen ouderen en jongeren heeft geïdentificeerd patiënten. Metformine mag alleen worden gebruikt bij patiënten met een normale nierfunctie. De initiële en onderhoudsdosering van metformine moet conservatief zijn bij patiënten met gevorderde leeftijd, vanwege het potentieel voor verminderde nierfunctie in deze populatie. Elke dosisaanpassing moet gebaseerd zijn op een zorgvuldige beoordeling van de nierfunctie. [Zien Contra; Waarschuwingen en voorzorgsmaatregelen; en Klinische Farmacologie.]
top
Overdose
sitagliptine
Tijdens gecontroleerde klinische onderzoeken bij gezonde personen werden enkele doses tot 800 mg sitagliptine toegediend. Maximale gemiddelde toenames in QTc van 8,0 msec werden waargenomen in één onderzoek bij een dosis van 800 mg sitagliptine, een gemiddeld effect dat niet klinisch belangrijk wordt geacht [zie Klinische Farmacologie]. Er is geen ervaring met doses hoger dan 800 mg bij mensen. In fase I-onderzoeken met meerdere doses werden geen dosisgerelateerde klinische bijwerkingen waargenomen met sitagliptine met doses tot 400 mg per dag gedurende een periode van maximaal 28 dagen.
In het geval van een overdosis is het redelijk om de gebruikelijke ondersteunende maatregelen te nemen, bijvoorbeeld het verwijderen van niet-geabsorbeerd materiaal uit het maagdarmkanaal darmkanaal, gebruik klinische monitoring (inclusief het verkrijgen van een elektrocardiogram) en stel ondersteunende therapie in zoals aangegeven door de klinische toestand.
Sitagliptine is bescheiden dialyseerbaar. In klinische onderzoeken werd ongeveer 13,5% van de dosis verwijderd gedurende een hemodialysesessie van 3 tot 4 uur. Langdurige hemodialyse kan worden overwogen indien klinisch aangewezen. Het is niet bekend of sitagliptine dialyseerbaar is door peritoneale dialyse.
Metformin hydrochloride
Er is een overdosis metforminehydrochloride opgetreden, inclusief inname van hoeveelheden van meer dan 50 gram. Hypoglykemie werd in ongeveer 10% van de gevallen gemeld, maar er is geen oorzakelijk verband met metforminehydrochloride vastgesteld. Lactaatacidose is gemeld in ongeveer 32% van de gevallen van overdosering met metformine [zie Waarschuwingen en voorzorgsmaatregelen]. Metformine is dialyseerbaar met een klaring tot 170 ml / min onder goede hemodynamische omstandigheden. Daarom kan hemodialyse nuttig zijn voor het verwijderen van geaccumuleerd geneesmiddel bij patiënten bij wie een overdosis metformine wordt vermoed.
top
Beschrijving
Janumet (sitagliptine / metformine HCl) tabletten bevatten twee orale antihyperglycemische geneesmiddelen die worden gebruikt bij de behandeling van diabetes type 2: sitagliptine en metforminehydrochloride.
sitagliptine
Sitagliptine is een oraal actieve remmer van het dipeptidylpeptidase-4 (DPP-4) -enzym. Sitagliptine is aanwezig in Janumet-tabletten in de vorm van sitagliptinefosfaatmonohydraat. Sitagliptinefosfaatmonohydraat wordt chemisch beschreven als 7 - [(3R) - 3 - amino - 1 - oxo - 4 - (2,4,5 - trifluorfenyl) butyl] - 5,6,7,8 - tetrahydro - 3 - (trifluormethyl) - 1,2,4 - triazolo [4,3 - a] pyrazinefosfaat (1: 1) monohydraat met een empirische formule van C16H15F6N5OH3PO4-H2O en een molecuulgewicht van 523,32. De structuurformule is:
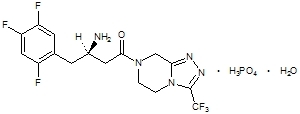
Sitagliptinefosfaatmonohydraat is een wit tot gebroken wit, kristallijn, niet-hygroscopisch poeder. Het is oplosbaar in water en N, N-dimethylformamide; enigszins oplosbaar in methanol; zeer weinig oplosbaar in ethanol, aceton en acetonitril; en onoplosbaar in isopropanol en isopropylacetaat.
Metformin hydrochloride
Metforminehydrochloride (N, N-dimethylimidodicarbonimidische diamidehydrochloride) is niet chemisch of farmacologisch gerelateerd aan andere klassen van orale antihyperglycemische middelen. Metforminehydrochloride is een witte tot gebroken witte kristallijne verbinding met een molecuulformule van C4H11N5-HCI en een molecuulgewicht van 165,63. Metforminehydrochloride is vrij oplosbaar in water en is praktisch onoplosbaar in aceton, ether en chloroform. De pKeen van metformine is 12.4. De pH van een 1% waterige oplossing van metforminehydrochloride is 6,68. De structuurformule is zoals weergegeven:
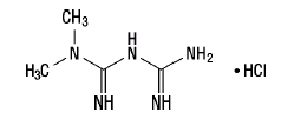
Janumet
Janumet is beschikbaar voor orale toediening als tabletten die 64,25 mg sitagliptinefosfaatmonohydraat en metforminehydrochloride-equivalent bevatten tot: 50 mg sitagliptine als vrije base en 500 mg metforminehydrochloride (Janumet 50 mg / 500 mg) of 1000 mg metforminehydrochloride (Janumet 50 mg / 1000 mg). Elke filmomhulde tablet Janumet bevat de volgende inactieve ingrediënten: microkristallijne cellulose, polyvinylpyrrolidon, natriumlaurylsulfaat en natriumstearylfumaraat. Bovendien bevat de filmcoating de volgende inactieve ingrediënten: polyvinylalcohol, polyethyleenglycol, talk, titaniumdioxide, rood ijzeroxide en zwart ijzeroxide.
top
Klinische Farmacologie
Werkingsmechanisme
Janumet
Janumet combineert twee antihyperglycemische middelen met complementaire werkingsmechanismen om de glykemische controle bij patiënten met diabetes type 2: sitagliptine, een dipeptidylpeptidase-4 (DPP-4) -remmer en metforminehydrochloride, een lid van de biguanide klasse.
sitagliptine
Sitagliptine is een DPP-4-remmer, waarvan wordt aangenomen dat het zijn werking uitoefent bij patiënten met diabetes type 2 door de inactivering van incretinehormonen te vertragen. Concentraties van de actieve intacte hormonen worden verhoogd door sitagliptine, waardoor de werking van deze hormonen wordt verhoogd en verlengd. Incretin-hormonen, waaronder glucagon-achtige peptide-1 (GLP-1) en glucoseafhankelijke insulinotrope polypeptide (GIP), worden de hele dag door de darm vrijgegeven en de niveaus stijgen als reactie naar een maaltijd. Deze hormonen worden snel geïnactiveerd door het enzym DPP-4. De incretines maken deel uit van een endogeen systeem dat betrokken is bij de fysiologische regulatie van glucosehomeostase. Wanneer de bloedglucoseconcentraties normaal of verhoogd zijn, verhogen GLP-1 en GIP de insulinesynthese en afgifte van pancreatische bètacellen door intracellulaire signaalroutes met cyclisch AMP. GLP-1 verlaagt ook glucagonafscheiding uit pancreas-alfacellen, wat leidt tot verminderde productie van glucose aan de lever. Door actieve incretinespiegels te verhogen en te verlengen, verhoogt sitagliptine de insulineafgifte en verlaagt het glucagonspiegels in de bloedsomloop op een glucoseafhankelijke manier. Sitagliptine vertoont selectiviteit voor DPP-4 en remt DPP-8 of DPP-9-activiteit niet in vitro in concentraties die die van therapeutische doses benaderen.
Metformin hydrochloride
Metformine is een antihyperglycemisch middel dat de glucosetolerantie verbetert bij patiënten met diabetes type 2, waardoor zowel basale als postprandiale plasmaglucose wordt verlaagd. De farmacologische werkingsmechanismen verschillen van andere klassen orale antihyperglycemische middelen. Metformine vermindert de glucoseproductie in de lever, vermindert de intestinale absorptie van glucose en verbetert de insulinegevoeligheid door de opname en het gebruik van perifere glucose te verhogen. In tegenstelling tot sulfonylureumderivaten veroorzaakt metformine geen hypoglykemie bij patiënten met diabetes type 2 of bij normale personen (behalve in speciale omstandigheden [zie Waarschuwingen en voorzorgsmaatregelen]) en veroorzaakt geen hyperinsulinemie. Bij metformine-therapie blijft de insulinesecretie onveranderd, terwijl nuchtere insulinespiegels en de insulinerespons van een dag lang mogelijk afnemen.
12.2 Farmacodynamiek
sitagliptine
Algemeen
Bij patiënten met diabetes type 2 leidde toediening van sitagliptine tot een remming van de DPP-4-enzymactiviteit gedurende een periode van 24 uur. Na een orale glucosebelasting of een maaltijd resulteerde deze DPP-4-remming in een 2- tot 3-voudige toename van de circulerende niveaus van actieve GLP-1 en GIP, verlaagde glucagonconcentraties en verhoogde responsiviteit van insulineafgifte op glucose, resulterend in hogere C-peptide en insuline concentraties. De toename van insuline met de afname van glucagon werd geassocieerd met lagere nuchtere glucoseconcentraties en verminderde glucose-excursie na een orale glucosebelasting of een maaltijd.
Sitagliptine en metforminehydrochloride Gelijktijdige toediening
In een tweedaags onderzoek bij gezonde proefpersonen verhoogde sitagliptine alleen de actieve GLP-1-concentraties, terwijl metformine alleen de actieve en totale GLP-1-concentraties in vergelijkbare mate verhoogde. Gelijktijdige toediening van sitagliptine en metformine had een additief effect op actieve GLP-1-concentraties. Sitagliptine, maar niet metformine, verhoogde actieve GIP-concentraties. Het is onduidelijk wat deze bevindingen betekenen voor veranderingen in de glykemische controle bij patiënten met diabetes type 2.
In onderzoeken met gezonde proefpersonen verlaagde sitagliptine de bloedglucose niet of veroorzaakte het hypoglykemie.
Cardiale elektrofysiologie
In een gerandomiseerd, placebo-gecontroleerd crossover-onderzoek kregen 79 gezonde proefpersonen een enkele orale dosis sitagliptine 100 mg, sitagliptine 800 mg (8 keer de aanbevolen dosis) en placebo toegediend. Bij de aanbevolen dosis van 100 mg was er geen effect op het QTc-interval verkregen bij de piekplasmaconcentratie of op enig ander moment tijdens het onderzoek. Na de dosis van 800 mg was de maximale toename van de placebo-gecorrigeerde gemiddelde verandering in QTc ten opzichte van de uitgangswaarde 3 uur na de dosis 8,0 msec. Deze toename wordt niet als klinisch significant beschouwd. Bij de dosis van 800 mg waren de piekplasmaconcentraties van sitagliptine ongeveer 11 keer hoger dan de piekconcentraties na een dosis van 100 mg.
Bij patiënten met diabetes type 2 die dagelijks sitagliptine 100 mg (N = 81) of sitagliptine 200 mg (N = 63) krijgen toegediend, is er waren geen betekenisvolle veranderingen in het QTc-interval op basis van ECG-gegevens verkregen ten tijde van het verwachte piekplasma concentratie.
farmacokinetiek
Janumet
De resultaten van een bio-equivalentieonderzoek bij gezonde proefpersonen toonden aan dat de Janumet (sitagliptine / metformine HCl) 50 mg / 500 mg en 50 mg / 1000 mg combinatietabletten zijn bio-equivalent aan gelijktijdige toediening van overeenkomstige doses sitagliptine (JANUVIA™2) en metforminehydrochloride als individuele tabletten.
Absorptie
sitagliptine
De absolute biologische beschikbaarheid van sitagliptine is ongeveer 87%. Gelijktijdige toediening van een vetrijke maaltijd met sitagliptine had geen effect op de farmacokinetiek van sitagliptine.
Metformin hydrochloride
De absolute biologische beschikbaarheid van een metforminehydrochloride-tablet van 500 mg onder nuchtere omstandigheden is ongeveer 50-60%. Studies met enkelvoudige orale doses van 500 mg tot 1500 mg metformine en 850 mg tot 2550 mg geven aan dat er een gebrek aan dosisproportionaliteit bij toenemende doses, die te wijten is aan verminderde absorptie in plaats van een wijziging in eliminatie. Voedsel vermindert de mate van en vertraagt de absorptie van metformine enigszins, zoals blijkt uit een ongeveer 40% lagere gemiddelde piekplasmaconcentratie (Cmax), een 25% lager gebied onder de plasmaconcentratie versus tijdcurve (AUC), en een verlenging van de tijd tot piekplasmaconcentratie met 35 minuten (Tmax) na toediening van een enkele tablet van 850 mg metformine met voedsel, vergeleken met dezelfde nuchtere tabletsterkte. De klinische relevantie van deze dalingen is onbekend.
Distributie
sitagliptine
Het gemiddelde distributievolume bij steady-state na een enkele intraveneuze dosis sitagliptine 100 mg aan gezonde proefpersonen is ongeveer 198 liter. De fractie sitagliptine reversibel gebonden aan plasma-eiwitten is laag (38%).
Metformin hydrochloride
Het schijnbare distributievolume (V / F) van metformine na enkele orale doses van 850 mg metforminehydrochloride gemiddeld 654 ± 358 L. Metformine is verwaarloosbaar gebonden aan plasma-eiwitten, in tegenstelling tot sulfonylurea, die voor meer dan 90% aan eiwitten zijn gebonden. Metformine verdeelt zich in erytrocyten, hoogstwaarschijnlijk als een functie van de tijd. Bij gebruikelijke klinische doses en doseringsschema's van metforminehydrochloride-tabletten worden steady-state plasmaconcentraties van metformine bereikt binnen 24-48 uur en zijn over het algemeen
Metabolisme
sitagliptine
Ongeveer 79% van sitagliptine wordt onveranderd uitgescheiden in de urine, waarbij metabolisme een ondergeschikte eliminatieroute is.
Na een [14C] sitagliptine orale dosis, ongeveer 16% van de radioactiviteit werd uitgescheiden als metabolieten van sitagliptine. Zes metabolieten werden op sporenniveau gedetecteerd en zullen naar verwachting niet bijdragen aan de plasma DPP-4-remmende activiteit van sitagliptine. In vitro-onderzoeken gaven aan dat het primaire enzym dat verantwoordelijk is voor het beperkte metabolisme van sitagliptine CYP3A4 was, met bijdrage van CYP2C8.
Metformin hydrochloride
Intraveneuze onderzoeken met eenmalige dosis bij normale proefpersonen tonen aan dat metformine onveranderd wordt uitgescheiden in de urine en ondergaat geen metabolisme in de lever (geen metabolieten zijn geïdentificeerd bij de mens) noch gal excretie.
afscheiding
sitagliptine
Na toediening van een orale [14C] sitagliptine dosis voor gezonde proefpersonen, ongeveer 100% van de toegediende radioactiviteit werd binnen een week na toediening geëlimineerd in feces (13%) of urine (87%). De schijnbare terminal t1/2 na een orale dosis van 100 mg sitagliptine was ongeveer 12,4 uur en de nierklaring was ongeveer 350 ml / min.
Eliminatie van sitagliptine vindt voornamelijk plaats via renale excretie en omvat actieve tubulaire secretie. Sitagliptine is een substraat voor humaan organisch aniontransporter-3 (hOAT-3), dat mogelijk betrokken is bij de renale eliminatie van sitagliptine. De klinische relevantie van hOAT-3 voor het transport van sitagliptine is niet vastgesteld. Sitagliptine is ook een substraat van p-glycoproteïne, dat mogelijk ook betrokken is bij de bemiddeling bij de renale eliminatie van sitagliptine. Cyclosporine, een p-glycoproteïne-remmer, verminderde echter de renale klaring van sitagliptine niet.
Metformin hydrochloride
De renale klaring is ongeveer 3,5 keer groter dan de creatinineklaring, wat aangeeft dat tubulaire secretie de belangrijkste eliminatieroute is. Na orale toediening wordt ongeveer 90% van het geabsorbeerde geneesmiddel binnen de eerste 24 uur via de nierroute geëlimineerd, met een plasma-eliminatiehalfwaardetijd van ongeveer 6,2 uur. In bloed is de eliminatiehalfwaardetijd ongeveer 17,6 uur, wat suggereert dat de erytrocytmassa een verdelingscompartiment kan zijn.
Speciale populaties
Nierinsufficiëntie
Janumet
Janumet mag niet worden gebruikt bij patiënten met nierinsufficiëntie [zie Contra; Waarschuwingen en voorzorgsmaatregelen].
sitagliptine
Een ongeveer 2-voudige toename van de plasma-AUC van sitagliptine werd waargenomen bij patiënten met matige nierinsufficiëntie en een ongeveer 4-voudige toename werd waargenomen bij patiënten met ernstige nierinsufficiëntie, waaronder patiënten met ESRD op hemodialyse, in vergelijking met normale gezonde controle onderwerpen.
Metformin hydrochloride
Bij patiënten met een verminderde nierfunctie (gebaseerd op gemeten creatinineklaring), de plasma- en bloedhalfwaardetijd van metformine is verlengd en de renale klaring is afgenomen evenredig met de afname van creatinine klaring.
Leverinsufficiëntie
sitagliptine
Bij patiënten met matige leverinsufficiëntie (Child-Pugh-score 7 tot 9), gemiddelde AUC en Cmax van sitagliptine steeg met respectievelijk ongeveer 21% en 13% in vergelijking met gezonde gematchte controles na toediening van een enkele dosis sitagliptine van 100 mg. Deze verschillen worden niet als klinisch relevant beschouwd.
Er is geen klinische ervaring bij patiënten met ernstige leverinsufficiëntie (Child-Pugh-score> 9).
Metformin hydrochloride
Er zijn geen farmacokinetische onderzoeken met metformine uitgevoerd bij patiënten met leverinsufficiëntie.
Geslacht
sitagliptine
Geslacht had geen klinisch betekenisvol effect op de farmacokinetiek van sitagliptine op basis van een composiet analyse van Fase I farmacokinetische gegevens en op een populatie farmacokinetische analyse van Fase I en Fase II gegevens.
Metformin hydrochloride
De farmacokinetische parameters van metformine verschilden niet significant tussen normale personen en patiënten met type 2-diabetes bij analyse op basis van geslacht. Evenzo was in gecontroleerde klinische onderzoeken bij patiënten met diabetes type 2 het antihyperglycemische effect van metformine vergelijkbaar bij mannen en vrouwen.
geriatrisch
sitagliptine
Wanneer rekening wordt gehouden met de effecten van leeftijd op de nierfunctie, had leeftijd alleen geen klinisch effect betekenisvolle impact op de farmacokinetiek van sitagliptine op basis van een populatiefarmacokinetiek analyse. Oudere personen (65 tot 80 jaar) hadden ongeveer 19% hogere plasmaconcentraties van sitagliptine in vergelijking met jongere personen.
Metformin hydrochloride
Beperkte gegevens uit gecontroleerde farmacokinetische studies van metformine bij gezonde oudere personen suggereren dat de totale plasmaklaring van metformine is verminderd, de halfwaardetijd is verlengd en Cmax is toegenomen in vergelijking met gezonde jonge proefpersonen. Uit deze gegevens blijkt dat de verandering in de farmacokinetiek van metformine in de eerste plaats wordt verklaard door een verandering in de nierfunctie (zie GLUCOPHAGE3 voorschrift informatie: KLINISCHE FARMACOLOGIE, Special Populations, Geriatrics).
Behandeling met Janumet mag niet worden gestart bij patiënten van ‰ ¥ 80 jaar, tenzij meting van de creatinineklaring aantoont dat de nierfunctie niet is verminderd [zie Waarschuwingen en voorzorgsmaatregelen].
Pediatric
Er zijn geen studies met Janumet uitgevoerd bij pediatrische patiënten.
Ras
sitagliptine
Ras had geen klinisch betekenisvol effect op de farmacokinetiek van sitagliptine op basis van een samengestelde analyse van beschikbare farmacokinetische gegevens, waaronder onderwerpen als wit, Spaans, zwart, Aziatisch en andere rassen groepen.
Metformin hydrochloride
Er zijn geen onderzoeken naar farmacokinetische parameters van metformine volgens ras uitgevoerd. In gecontroleerde klinische onderzoeken met metformine bij patiënten met diabetes type 2 was het antihyperglycemische effect vergelijkbaar bij blanken (n = 249), zwarten (n = 51) en Hispanics (n = 24).
Body Mass Index (BMI)
sitagliptine
Body mass index had geen klinisch betekenisvol effect op de farmacokinetiek van sitagliptine op basis van een composiet analyse van Fase I farmacokinetische gegevens en op een populatie farmacokinetische analyse van Fase I en Fase II gegevens.
Geneesmiddelinteracties
Sitagliptine en metforminehydrochloride
Gelijktijdige toediening van meerdere doses sitagliptine (50 mg) en metformine (1000 mg) tweemaal daags gedaan de farmacokinetiek van sitagliptine of metformine niet significant veranderen bij patiënten met type 2 diabetes.
Er zijn geen farmacokinetische geneesmiddeleninteractiestudies met Janumet uitgevoerd; dergelijke onderzoeken zijn echter uitgevoerd met de afzonderlijke componenten van Janumet (sitagliptine en metforminehydrochloride).
sitagliptine
In vitro beoordeling van geneesmiddelinteracties
Sitagliptine is geen remmer van CYP-isozymen CYP3A4, 2C8, 2C9, 2D6, 1A2, 2C19 of 2B6 en is geen inductor van CYP3A4. Sitagliptine is een p-glycoproteïne-substraat, maar remt niet door p-glycoproteïne gemedieerd transport van digoxine. Op basis van deze resultaten wordt het onwaarschijnlijk geacht dat sitagliptine interacties veroorzaakt met andere geneesmiddelen die deze routes gebruiken.
Sitagliptine is niet uitgebreid gebonden aan plasma-eiwitten. Daarom is de neiging van sitagliptine om betrokken te zijn bij klinisch betekenisvolle geneesmiddel-geneesmiddelinteracties gemedieerd door plasma-eiwitbindingsverplaatsing zeer laag.
In vivo beoordeling van geneesmiddelinteracties
Effect van sitagliptine op andere geneesmiddelen
In klinische onderzoeken, zoals hieronder beschreven, veranderde sitagliptine de farmacokinetiek van metformine, glyburide, simvastatine, rosiglitazon, warfarine of oraal niet significant anticonceptiemiddelen, die in vivo bewijs leveren van een lage neiging om geneesmiddelinteracties te veroorzaken met substraten van CYP3A4, CYP2C8, CYP2C9 en organische kationische transporter (Oktober).
Digoxine: Sitagliptine had een minimaal effect op de farmacokinetiek van digoxine. Na toediening van 0,25 mg digoxine gelijktijdig met 100 mg sitagliptine dagelijks gedurende 10 dagen, was de plasma-AUC van digoxine verhoogd met 11% en de plasma-Cmax met 18%.
Sulfonylureumderivaten: de farmacokinetiek van eenmalige dosis glyburide, een CYP2C9-substraat, was niet significant gewijzigd bij personen die meerdere doses sitagliptine kregen. Klinisch relevante interacties worden niet verwacht met andere sulfonylureumderivaten (bijv. Glipizide, tolbutamide en glimepiride) die, net als glyburide, voornamelijk worden geëlimineerd door CYP2C9 [zie Waarschuwingen en voorzorgsmaatregelen].
Simvastatine: De farmacokinetiek van eenmalige dosis simvastatine, een CYP3A4-substraat, was niet betekenisvol veranderd bij personen die meerdere dagelijkse doses sitagliptine kregen. Daarom is sitagliptine geen remmer van CYP3A4-gemedieerd metabolisme.
Thiazolidinediones: de farmacokinetiek van eenmalige dosis rosiglitazon was bij patiënten niet significant veranderd meerdere dagelijkse doses sitagliptine krijgen, wat aangeeft dat sitagliptine geen remmer is van CYP2C8-gemedieerd metabolisme.
Warfarine: Meerdere dagelijkse doses sitagliptine veranderden de farmacokinetiek niet op significante wijze, zoals bepaald door meting van S (-) of R (+) warfarine enantiomeren, of farmacodynamiek (zoals beoordeeld door meting van protrombine INR) van een enkele dosis warfarine. Omdat S (-) warfarine voornamelijk wordt gemetaboliseerd door CYP2C9, ondersteunen deze gegevens ook de conclusie dat sitagliptine geen CYP2C9-remmer is.
Orale anticonceptiva: Gelijktijdige toediening met sitagliptine veranderde de steady-state farmacokinetiek van norethindron of ethinylestradiol niet significant.
Effect van andere geneesmiddelen op sitagliptine
Klinische gegevens hieronder beschreven suggereren dat sitagliptine niet gevoelig is voor klinisch betekenisvolle interacties door gelijktijdig toegediende medicijnen.
Cyclosporine: Er is een studie uitgevoerd om het effect van cyclosporine, een krachtige remmer van p-glycoproteïne, op de farmacokinetiek van sitagliptine te beoordelen. Gelijktijdige toediening van een enkele orale dosis sitagliptine 100 mg en een enkele orale dosis cyclosporine 600 mg verhoogde de AUC en Cmax van sitagliptine met respectievelijk ongeveer 29% en 68%. Deze bescheiden veranderingen in de farmacokinetiek van sitagliptine werden niet als klinisch relevant beschouwd. De renale klaring van sitagliptine was ook niet betekenisvol veranderd. Daarom worden geen betekenisvolle interacties verwacht met andere p-glycoproteïne-remmers.
Metformin hydrochloride
[Zien Geneesmiddelinteracties]
top
Niet-klinische Toxicologie
Carcinogenese, mutagenese, aantasting van de vruchtbaarheid
Janumet
Er zijn geen dierstudies uitgevoerd met de gecombineerde producten in Janumet om carcinogenese, mutagenese of verminderde vruchtbaarheid te evalueren. De volgende gegevens zijn gebaseerd op de bevindingen in onderzoeken met sitagliptine en metformine afzonderlijk.
sitagliptine
Een tweejarig carcinogeniteitsonderzoek is uitgevoerd bij mannelijke en vrouwelijke ratten die orale doses sitagliptine kregen van 50, 150 en 500 mg / kg / dag. Er was een verhoogde incidentie van gecombineerd leveradenoom / carcinoom bij mannen en vrouwen en van levercarcinoom bij vrouwen bij 500 mg / kg. Deze dosis resulteert in blootstellingen van ongeveer 60 keer de menselijke blootstelling bij de maximale aanbevolen dagelijkse dosis voor volwassenen (MRHD) voor volwassenen van 100 mg / dag op basis van AUC-vergelijkingen. Levertumoren werden niet waargenomen bij 150 mg / kg, ongeveer 20 keer de menselijke blootstelling bij de MRHD. Een tweejarig carcinogeniciteitsonderzoek werd uitgevoerd bij mannelijke en vrouwelijke muizen die orale doses sitagliptine kregen van 50, 125, 250 en 500 mg / kg / dag. Er was geen toename in de incidentie van tumoren in elk orgaan tot 500 mg / kg, ongeveer 70 keer de menselijke blootstelling bij de MRHD. Sitagliptine was niet mutageen of clastogeen met of zonder metabole activering in de Ames bacteriële mutageniteitstest, een Chinese hamsterovarium (CHO) chromosoomafwijkingstest, een in vitro cytogenetica-test in CHO, een in vitro rattenhepatocyt DNA alkalische elutietest en een in vivo micronucleus assay.
In vruchtbaarheidsstudies bij ratten met doses voor orale sondes van 125, 250 en 1000 mg / kg werden mannen gedurende 4 weken voorafgaand aan de paring behandeld, tijdens paring, tot geplande beëindiging (in totaal ongeveer 8 weken), en vrouwen werden 2 weken voorafgaand aan de paring behandeld door dracht dag 7. Er werd geen nadelig effect op de vruchtbaarheid waargenomen bij 125 mg / kg (ongeveer 12 keer menselijke blootstelling bij de MRHD van 100 mg / dag op basis van AUC-vergelijkingen). Bij hogere doses werden niet-dosis-gerelateerde verhoogde resorpties bij vrouwen waargenomen (ongeveer 25 en 100 keer menselijke blootstelling bij de MRHD op basis van AUC-vergelijking).
Metformin hydrochloride
Lange termijn carcinogeniteitsstudies zijn uitgevoerd bij ratten (doseringsduur van 104 weken) en muizen (doseringsduur van 91 weken) bij doses tot en met 900 mg / kg / dag en 1500 mg / kg / dag, respectievelijk. Deze doses zijn beide ongeveer vier keer de maximale aanbevolen dagelijkse menselijke dosis van 2000 mg op basis van vergelijkingen van het lichaamsoppervlak. Bij mannelijke of vrouwelijke muizen zijn geen aanwijzingen gevonden voor carcinogeniteit met metformine. Evenzo werd er geen mannelijk potentieel waargenomen met metformine bij mannelijke ratten. Er was echter een verhoogde incidentie van goedaardige stromale uteriene poliepen bij vrouwelijke ratten die werden behandeld met 900 mg / kg / dag.
Er waren geen aanwijzingen voor een mutageen potentieel van metformine in de volgende in-vitrotests: Ames-test (S. typhimurium), genmutatietest (lymfoomcellen van muizen) of chromosomale aberratietest (menselijke lymfocyten). De resultaten in de in vivo micronucleustest bij muizen waren ook negatief. De vruchtbaarheid van mannelijke of vrouwelijke ratten werd niet beïnvloed door metformine bij toediening in doses van maximaal 600 mg / kg / dag, die ongeveer drie keer de maximale aanbevolen dagelijkse dosis voor mensen is, gebaseerd op het lichaamsoppervlak vergelijkingen.
top
Klinische studies
De gelijktijdige toediening van sitagliptine en metformine is onderzocht bij patiënten met diabetes type 2 die onvoldoende gecontroleerd werden op dieet en lichaamsbeweging en in combinatie met glimepiride.
Er zijn geen klinische werkzaamheidsstudies uitgevoerd met Janumet; de bio-equivalentie van Janumet met gelijktijdig toegediende sitagliptine en metforminehydrochloride-tabletten werd echter aangetoond.
Sitagliptine en metformine Gelijktijdige toediening bij patiënten met diabetes type 2 onvoldoende gecontroleerd op dieet en lichaamsbeweging
In totaal namen 1091 patiënten met diabetes type 2 en onvoldoende glykemische controle op dieet en lichaamsbeweging deel aan een 24-weken durende, gerandomiseerde, dubbelblinde, placebo-gecontroleerde factoriële studie ontworpen om de werkzaamheid van sitagliptine en metformine te beoordelen gelijktijdige toediening. Patiënten met een antihyperglycemisch middel (N = 541) ondergingen een dieet, lichaamsbeweging en uitwasperiode van geneesmiddelen van maximaal 12 weken. Na de uitwasperiode werden patiënten met onvoldoende glykemische controle (A1C 7,5% tot 11%) gerandomiseerd na het voltooien van een enkelblinde placebo-inloopperiode van 2 weken. Patiënten die geen antihyperglycemische middelen gebruiken bij binnenkomst van het onderzoek (N = 550) met onvoldoende glykemische controle (A1C 7,5% tot 11%) ging onmiddellijk de 2 weken durende single-blind placebo-inloopperiode in en vervolgens waren gerandomiseerd. Ongeveer gelijke aantallen patiënten werden gerandomiseerd om placebo, 100 mg sitagliptine eenmaal daags, 500 mg of 1000 te ontvangen mg metformine tweemaal daags, of 50 mg sitagliptine tweemaal daags in combinatie met 500 mg of 1000 mg metformine tweemaal daags dagelijks. Patiënten die tijdens het onderzoek niet aan specifieke glycemische doelen voldeden, werden behandeld met glyburide (glibenclamide) rescue.
Gelijktijdige toediening van sitagliptine en metformine zorgde voor significante verbeteringen in A1C, FPG en PPG van 2 uur vergeleken met placebo, alleen metformine en alleen sitagliptine (tabel 3, figuur 1). Gemiddelde reducties ten opzichte van baseline in A1C waren over het algemeen groter voor patiënten met hogere baseline A1C-waarden. Voor patiënten die bij aanvang van de studie geen antihyperglycemisch middel gebruikten, waren de gemiddelde verminderingen ten opzichte van de uitgangswaarde bij A1C: sitagliptine 100 mg eenmaal daags, -1,1%; metformine 500 mg bid, -1,1%; metformine 1000 mg bid, -1,2%; sitagliptine 50 mg bid met metformine 500 mg bid, -1,6%; sitagliptine 50 mg bid met metformine 1000 mg bid, -1,9%; en voor patiënten die placebo kregen, -0,2%. Lipide-effecten waren over het algemeen neutraal. De afname van het lichaamsgewicht in de groepen die sitagliptine kregen in combinatie met metformine was vergelijkbaar met die in de groepen die alleen metformine of placebo kregen.
Tabel 3: Glycemische parameters bij eindbezoek (24-weken durende studie) voor Sitagliptin en Metformin, alleen en in combinatie bij patiënten met diabetes type 2 onvoldoende gecontroleerd op dieet en lichaamsbeweging *
Placebo |
sitagliptine 100 mg QD |
metformine 500 mg bid |
metformine 1000 mg bid |
sitagliptine 50 mg bid + metformine 500 mg bid |
sitagliptine 50 mg bid + metformine 1000 mg bid |
|
| ||||||
| A1C (%) | N = 165 | N = 175 | N = 178 | N = 177 | N = 183 | N = 178 |
| Baseline (gemiddelde) | 8.7 | 8.9 | 8.9 | 8.7 | 8.8 | 8.8 |
| Verandering van baseline (aangepast gemiddelde†) | 0.2 | -0.7 | -0.8 | -1.1 | -1.4 | -1.9 |
| Verschil met placebo (aangepast gemiddelde†) (95% BI) |
-0.8c (-1.1, -0.6) |
-1.0c (-1.2, -0.8) |
-1.3c (-1.5, -1.1) |
-1.6c (-1.8, -1.3) |
-2.1c (-2.3, -1.8) |
|
| Patiënten (%) die A1C <7% behalen | 15 (9%) | 35 (20%) | 41 (23%) | 68 (38%) | 79 (43%) | 118 (66%) |
| % Patiënten die reddingsmedicatie ontvangen | 32 | 21 | 17 | 12 | 8 | 2 |
| FPG (mg / dL) | N = 169 | N = 178 | N = 179 | N = 179 | N = 183 | N = 180 |
| Baseline (gemiddelde) | 196 | 201 | 205 | 197 | 204 | 197 |
| Verandering van baseline (aangepast gemiddelde†) | 6 | -17 | -27 | -29 | -47 | -64 |
| Verschil met placebo (aangepast gemiddelde†) (95% BI) |
-23c (-33, -14) |
-33c (-43, -24) |
-35c (-45, -26) |
-53c (-62, -43) |
-70c (-79, -60) |
|
| 2 uur PPG (mg / dL) | N = 129 | N = 136 | N = 141 | N = 138 | N = 147 | N = 152 |
| Baseline (gemiddelde) | 277 | 285 | 293 | 283 | 292 | 287 |
| Verandering van baseline (aangepast gemiddelde†) | 0 | -52 | -53 | -78 | -93 | -117 |
| Verschil met placebo (aangepast gemiddelde†) (95% BI) |
-52c (-67, -37) |
-54c (-69, -39) |
-78c (-93, -63) |
-93c (-107, -78) |
-117c (-131, -102) |
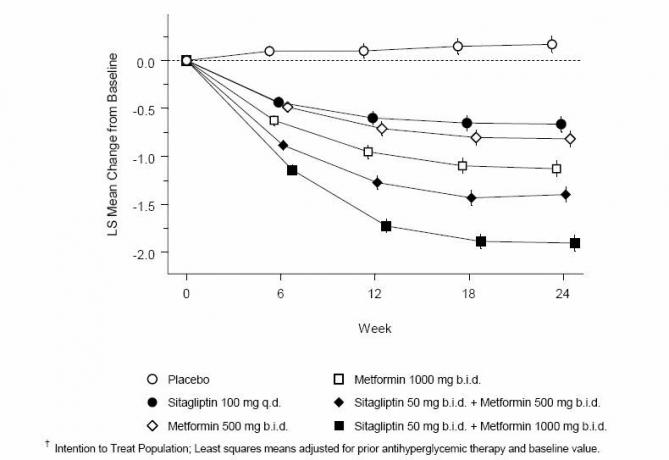
Figuur 1: Gemiddelde verandering ten opzichte van de uitgangswaarde voor A1C (%) gedurende 24 weken met alleen sitagliptine en metformine en in combinatie bij patiënten met diabetes type 2 onvoldoende gecontroleerd met dieet en lichaamsbewegingâ €
Bovendien omvatte deze studie patiënten (N = 117) met ernstigere hyperglycemie (A1C> 11% of bloed) glucose> 280 mg / dL) die werden behandeld met tweemaal daags open-label sitagliptine 50 mg en metformine 1000 mg. In deze groep patiënten was de gemiddelde baseline A1C-waarde 11,2%, was de gemiddelde FPG 314 mg / dL en was de gemiddelde PPG van 2 uur 441 mg / dL. Na 24 weken werden gemiddelde dalingen van de basislijn van -2,9% voor A1C, -127 mg / dL voor FPG en -208 mg / dL voor 2 uur PPG waargenomen.
De initiële combinatietherapie of het onderhoud van combinatietherapie moet worden geïndividualiseerd en worden overgelaten aan het oordeel van de zorgverlener.
Sitagliptine add-on therapie bij patiënten met diabetes type 2 Onvoldoende gecontroleerd met alleen metformine
In totaal namen 701 patiënten met type 2 diabetes deel aan een 24 weken durende, gerandomiseerde, dubbelblinde, placebo-gecontroleerde studie die was opgezet om de werkzaamheid van sitagliptine in combinatie met metformine te beoordelen. Patiënten die al metformine (N = 431) gebruikten in een dosis van ten minste 1500 mg per dag werden gerandomiseerd na het voltooien van een 2 weken durende, enkelblinde placebo-inloopperiode. Patiënten die metformine en een ander antihyperglycemisch middel gebruiken (N = 229) en patiënten die geen antihyperglycemische middelen gebruiken (uit therapie gedurende ten minste 8 weken, N = 41) werden gerandomiseerd na een inloopperiode van ongeveer 10 weken met metformine (bij een dosis van ten minste 1500 mg per dag) in monotherapie. Patiënten werden gerandomiseerd naar de toevoeging van ofwel 100 mg sitagliptine of placebo, eenmaal daags toegediend. Patiënten die tijdens de onderzoeken niet aan specifieke glycemische doelen voldeden, werden behandeld met pioglitazon rescue.
In combinatie met metformine zorgde sitagliptine voor significante verbeteringen in A1C, FPG en PPG van 2 uur in vergelijking met placebo met metformine (tabel 4). Rescue glycemische therapie werd gebruikt bij 5% van de patiënten behandeld met sitagliptine 100 mg en bij 14% van de patiënten behandeld met placebo. Een vergelijkbare afname in lichaamsgewicht werd waargenomen voor beide behandelingsgroepen.
Tabel 4: Glycemische parameters bij laatste bezoek (24 weken durende studie) van sitagliptine in aanvullende combinatietherapie met metformine *
| Sitagliptine 100 mg QD + Metformine |
Placebo + Metformine |
|
| ||
| A1C (%) | N = 453 | N = 224 |
| Baseline (gemiddelde) | 8.0 | 8.0 |
| Verandering van baseline (aangepast gemiddelde†) | -0.7 | -0.0 |
| Verschil met placebo + metformine (aangepast gemiddelde†) (95% BI) |
-0.7c (-0.8, -0.5) |
|
| Patiënten (%) die A1C <7% behalen | 213 (47%) | 41 (18%) |
| FPG (mg / dL) | N = 454 | N = 226 |
| Baseline (gemiddelde) | 170 | 174 |
| Verandering van baseline (aangepast gemiddelde†) | -17 | 9 |
| Verschil met placebo + metformine (aangepast gemiddelde†) (95% BI) |
-25c (-31, -20) |
|
| 2 uur PPG (mg / dL) | N = 387 | N = 182 |
| Baseline (gemiddelde) | 275 | 272 |
| Verandering van baseline (aangepast gemiddelde†) | -62 | -11 |
| Verschil met placebo + metformine (aangepast gemiddelde†) (95% BI) |
-51c (-61, -41) |
Sitagliptine add-on therapie bij patiënten met diabetes type 2 onvoldoende gecontroleerd op de combinatie van metformine en glimepiride
In totaal namen 441 patiënten met diabetes type 2 deel aan een 24-weken durende, gerandomiseerde, dubbelblinde, placebo-gecontroleerde studie ontworpen om de werkzaamheid van sitagliptine te beoordelen in combinatie met glimepiride, met of zonder metformine. Patiënten gingen een run-in behandelingsperiode in op glimepiride (â ‰ ¥ 4 mg per dag) alleen of glimepiride in combinatie met metformine (â ‰ ¥ 1500 mg per dag). Na een dosis-titratie en dosis-stabiele inloopperiode van maximaal 16 weken en een placebo-inloopperiode van 2 weken, patiënten met onvoldoende glycemische controle (A1C 7,5% tot 10,5%) werd gerandomiseerd naar de toevoeging van 100 mg sitagliptine of placebo, eenmaal toegediend dagelijks. Patiënten die tijdens de onderzoeken niet aan specifieke glycemische doelen voldeden, werden behandeld met pioglitazon rescue.
Patiënten die sitagliptine met metformine en glimepiride kregen, hadden significante verbeteringen in A1C en FPG in vergelijking met patiënten die placebo met metformine en glimepiride (tabel 5), met gemiddelde verlagingen ten opzichte van de uitgangswaarde ten opzichte van placebo in A1C van -0,9% en in FPG van -21 mg / dL. Reddingstherapie werd gebruikt bij 8% van de patiënten behandeld met sitagliptine 100 mg en 29% van de patiënten behandeld met add-on placebo. De patiënten behandeld met add-on sitagliptine hadden een gemiddelde toename van het lichaamsgewicht van 1,1 kg versus add-on placebo (+0,4 kg versus -0,7 kg). Bovendien resulteerde add-on sitagliptine in een verhoogde hypoglykemie in vergelijking met add-on placebo. [Zien Waarschuwingen en voorzorgsmaatregelen; Bijwerkingen.]
Tabel 5: Glycemische parameters bij laatste bezoek (24 weken durende studie) voor sitagliptine in combinatie met metformine en glimepiride *
| Sitagliptine 100 mg + Metformine en Glimepiride |
Placebo + Metformine en Glimepiride |
|
| ||
| A1C (%) | N = 115 | N = 105 |
| Baseline (gemiddelde) | 8.3 | 8.3 |
| Verandering van baseline (aangepast gemiddelde†) | -0.6 | 0.3 |
| Verschil met placebo (aangepast gemiddelde†) (95% BI) | -0.9c (-1.1, -0.7) |
|
| Patiënten (%) die A1C <7% behalen | 26 (23%) | 1 (1%) |
| FPG (mg / dL) | N = 115 | N = 109 |
| Baseline (gemiddelde) | 179 | 179 |
| Verandering van baseline (aangepast gemiddelde†) | -8 | 13 |
| Verschil met placebo (aangepast gemiddelde†) (95% BI) | -21c (-32, -10) |
Sitagliptin add-on therapie versus Glipizide add-on therapie bij patiënten met diabetes type 2 onvoldoende gecontroleerd op metformine
De werkzaamheid van sitagliptine werd geëvalueerd in een 52 weken durende, dubbelblinde, glipizide-gecontroleerde non-inferioriteitstudie bij patiënten met diabetes type 2. Patiënten die niet werden behandeld of andere antihyperglycemische middelen gebruikten, liepen een inloopperiode van maximaal 12 weken in met metformine monotherapie (dosis van â 1500 ¥ 1500 mg per dag) inclusief het wegspoelen van andere medicijnen dan metformine, als van toepassing. Na de inloopperiode werden degenen met onvoldoende glycemische controle (A1C 6,5% tot 10%) 1: 1 gerandomiseerd aan de toevoeging van sitagliptine 100 mg eenmaal daags of glipizide gedurende 52 weken. Patiënten die glipizide kregen, kregen een startdosis van 5 mg / dag en werden vervolgens gedurende de volgende 18 weken naar keuze getitreerd tot een maximale dosering van 20 mg / dag, indien nodig om de glykemische controle te optimaliseren. Daarna moest de dosis glipizide constant worden gehouden, behalve down-titratie om hypoglykemie te voorkomen. De gemiddelde dosis glipizide na de titratieperiode was 10 mg.
Na 52 weken hadden sitagliptine en glipizide vergelijkbare gemiddelde verminderingen ten opzichte van de uitgangswaarde in A1C in de intent-to-treat-analyse (tabel 6). Deze resultaten waren consistent met de analyse per protocol (figuur 2). Een conclusie ten gunste van de niet-inferioriteit van sitagliptine ten opzichte van glipizide kan beperkt zijn tot patiënten met baseline A1C vergelijkbaar met die opgenomen in de studie (meer dan 70% van de patiënten had baseline A1C <8% en meer dan 90% had A1C <9%).
Tabel 6: Glycemische parameters in een 52 weken durende studie waarin sitagliptine vergeleken wordt met glipizide als aanvullende therapie bij patiënten die onvoldoende gecontroleerd worden op metformine (populatie met intent-to-treat) *
| Sitagliptine 100 mg + Metformine |
glipizide + Metformine |
|
| ||
| A1C (%) | N = 576 | N = 559 |
| Baseline (gemiddelde) | 7.7 | 7.6 |
| Verandering van baseline (aangepast gemiddelde†) | -0.5 | -0.6 |
| FPG (mg / dL) | N = 583 | N = 568 |
| Baseline (gemiddelde) | 166 | 164 |
| Verandering van baseline (aangepast gemiddelde†) | -8 | -8 |

Figuur 2: Gemiddelde verandering ten opzichte van de uitgangswaarde voor A1C (%) Meer dan 52 weken in een studie waarin Sitagliptin werd vergeleken met Glipizide als aanvullende therapie bij patiënten die onvoldoende gecontroleerd worden op metformine (per protocolpopulatie) â€
De incidentie van hypoglykemie in de sitagliptinegroep (4,9%) was significant (p <0,001) lager dan die in de glipizidegroep (32,0%). Patiënten behandeld met sitagliptine vertoonden een significante gemiddelde afname ten opzichte van de uitgangswaarde in lichaamsgewicht in vergelijking met een significante gewichtstoename bij patiënten die glipizide kregen (-1,5 kg versus +1,1 kg).
top
Hoe geleverd
Nr. 6747 - Tabletten Janumet, 50 mg / 500 mg, zijn lichtroze, capsulevormige, filmomhulde tabletten met aan één zijde de inscriptie "575". Ze worden als volgt geleverd:
NDC 0006-0575-61 gebruikseenheid van 60 flessen
NDC 0006-0575-62 flacons van 180 eenheden
NDC 0006-0575-52 blisterverpakkingen met eenheidsdosis van 50
NDC 0006-0575-82 bulkflessen van 1000.
Nr. 6749 - Tabletten Janumet, 50 mg / 1000 mg, zijn rode, capsulevormige, filmomhulde tabletten met aan één zijde de inscriptie "577". Ze worden als volgt geleverd:
NDC 0006-0577-61 gebruikseenheid van 60 flessen
NDC 0006-0577-62 flacons van 180 eenheden
NDC 0006-0577-52 blisterverpakkingen met eenheidsdosis van 50
NDC 0006-0577-82 bulkflessen van 1000.
Bewaren bij 20-25 ° C (68-77 ° F), excursies toegestaan tot 15-30 ° C (59-86 ° F).
top
Informatie voor patiëntbegeleiding
Instructions
Patiënten moeten worden geïnformeerd over de mogelijke risico's en voordelen van Janumet en van alternatieve therapiemethoden. Ze moeten ook worden geïnformeerd over het belang van de naleving van voedingsinstructies, regelmatige lichamelijke activiteit, periodiek bloed glucosemonitoring en A1C-testen, herkenning en beheer van hypoglykemie en hyperglykemie en beoordeling van diabetes complicaties. Tijdens periodes van stress zoals koorts, trauma, infectie of chirurgie kunnen medicatievereisten veranderen en moeten patiënten worden geadviseerd om onmiddellijk medisch advies in te winnen.
De risico's van lactaatacidose als gevolg van de metforminecomponent, de symptomen en aandoeningen die vatbaar zijn voor de ontwikkeling ervan, zoals vermeld in Waarschuwingen en voorzorgsmaatregelen, moet worden uitgelegd aan patiënten. Patiënten moet worden geadviseerd om Janumet onmiddellijk te staken en hun arts onmiddellijk op de hoogte te stellen als onverklaarbare hyperventilatie, myalgie, malaise, ongewone slaperigheid, duizeligheid, trage of onregelmatige hartslag, een koud gevoel (vooral in de extremiteiten) of andere niet-specifieke symptomen optreden. Gastro-intestinale symptomen komen vaak voor tijdens de start van de behandeling met metformine en kunnen optreden tijdens de start van de behandeling met Janumet; patiënten moeten echter hun arts raadplegen als ze onverklaarbare symptomen ontwikkelen. Hoewel gastro-intestinale symptomen die optreden na stabilisatie waarschijnlijk geen verband houden met het geneesmiddel, is een dergelijke het optreden van symptomen moet worden geëvalueerd om te bepalen of dit te wijten is aan lactaatacidose of andere ernstige ziekte.
Patiënten moeten worden geadviseerd tegen overmatige alcoholinname, hetzij acuut of chronisch, tijdens het gebruik van Janumet.
Patiënten moeten worden geïnformeerd over het belang van het regelmatig testen van de nierfunctie en hematologische parameters bij behandeling met Janumet.
Patiënten moeten worden geïnformeerd dat allergische reacties zijn gemeld tijdens postmarketinggebruik van sitagliptine, een van de componenten van Janumet. Als symptomen van allergische reacties (waaronder uitslag, netelroos en zwelling van het gezicht, lippen, tong en keel problemen met ademhalen of slikken veroorzaken), moeten patiënten stoppen met het innemen van Janumet en medisch advies inwinnen onmiddellijk.
Artsen moeten hun patiënten opdragen de bijsluiter van de patiënt te lezen voordat ze met de Janumet-therapie beginnen en elke keer dat het recept wordt vernieuwd, opnieuw te lezen. Patiënten moeten worden geïnstrueerd om hun arts of apotheker op de hoogte te brengen als ze een ongebruikelijk symptoom ontwikkelen of als een bekend symptoom aanhoudt of verergert.
Laboratorium testen
De respons op alle diabetische therapieën moet worden gemonitord door periodieke metingen van bloedglucose en A1C-waarden, met als doel deze waarden te verlagen naar het normale bereik. A1C is vooral nuttig voor het evalueren van glykemische controle op lange termijn.
Eerste en periodieke monitoring van hematologische parameters (bijv. Hemoglobine / hematocriet en rood bloed celindices) en nierfunctie (serumcreatinine) moeten worden uitgevoerd, ten minste op jaarbasis. Hoewel megaloblastaire anemie zelden is gezien met metformine-therapie, moet vitamine B12-tekort worden uitgesloten als dit wordt vermoed.
Gedistribueerd door:
MERCK & CO., INC., Whitehouse Station, NJ 08889, VS.
9794108
Amerikaans octrooischrift: 6.699.871
1 Geregistreerd handelsmerk van MERCK & CO., Inc., Whitehouse Station, New Jersey 08889 USA
2 Handelsmerk van MERCK & CO., Inc., Whitehouse Station, New Jersey 08889 VS.
3GLUCOPHAGE® is een geregistreerd handelsmerk van Merck Sante S.A.S, een partner van Merck KGaA uit Darmstadt, Duitsland.
In licentie gegeven aan Bristol-Myers Squibb Company.
COPYRIGHT © 2007, 2008 MERCK & CO., Inc.
Alle rechten voorbehouden
FDA-goedgekeurde patiëntetikettering
Patiënt informatie
Janumet® (JAN-you-met)
(sitagliptine / metformine HCl)
Tablets
Lees de patiëntinformatie die bij Janumet1 wordt geleverd voordat u begint met innemen en telkens wanneer u een nieuwe vulling krijgt. Er kan nieuwe informatie zijn. Deze bijsluiter vervangt niet uw arts met uw medische toestand of behandeling.
Wat is de belangrijkste informatie die ik over Janumet moet weten?
Metforminehydrochloride, een van de ingrediënten in Janumet, kan een zeldzame maar ernstige bijwerking genaamd lactaatacidose (een opeenhoping van melkzuur in het bloed) veroorzaken die de dood kan veroorzaken. Lactaatacidose is een medisch noodgeval en moet in een ziekenhuis worden behandeld.
Stop met het innemen van Janumet en neem onmiddellijk contact op met uw arts als u een van de volgende symptomen van lactaatacidose krijgt:
- Je voelt je erg zwak en moe.
- U heeft ongewone (niet normale) spierpijn.
- Je hebt moeite met ademhalen.
- U heeft onverklaarbare maag- of darmproblemen met misselijkheid en braken of diarree.
- Je hebt het koud, vooral in je armen en benen.
- Je voelt je duizelig of licht in het hoofd.
- U heeft een langzame of onregelmatige hartslag.
U hebt een grotere kans om lactaatacidose te krijgen als u:
- nierproblemen heeft.
- leverproblemen heeft.
- congestief hartfalen heeft waarvoor behandeling met medicijnen nodig is.
- veel alcohol drinken (heel vaak of op korte termijn "binge" drinken).
- uitgedroogd raken (een grote hoeveelheid lichaamsvloeistoffen verliezen). Dit kan gebeuren als u ziek bent met koorts, braken of diarree. Uitdroging kan ook optreden als u veel zweet tijdens activiteiten of lichaamsbeweging en niet voldoende vocht drinkt.
- bepaalde röntgentests uitvoeren met injecteerbare kleurstoffen of contrastmiddelen.
- operatie ondergaan.
- een hartaanval, ernstige infectie of beroerte heeft.
- 80 jaar of ouder zijn en uw nierfunctie niet hebben getest.
Wat is Janumet?
Janumet-tabletten bevatten twee geneesmiddelen op recept, sitagliptine (JANUVIA ™ 2) en metformine. Janumet kan samen met dieet en lichaamsbeweging worden gebruikt om de bloedsuikerspiegel te verlagen bij volwassen patiënten met diabetes type 2. Uw arts zal bepalen of Janumet geschikt is voor u en zal de beste manier bepalen om uw diabetes te starten en te blijven behandelen.
Janumet:
- helpt om de insulinespiegels na een maaltijd te verbeteren.
- helpt het lichaam beter te reageren op de insuline die het op natuurlijke wijze aanmaakt.
- vermindert de hoeveelheid suiker die door het lichaam wordt gemaakt.
- het is onwaarschijnlijk dat het een lage bloedsuiker (hypoglykemie) veroorzaakt wanneer het zelf wordt ingenomen om een hoge bloedsuiker te behandelen.
Janumet is niet onderzocht bij kinderen jonger dan 18 jaar.
Janumet is niet onderzocht met insuline, een geneesmiddel waarvan bekend is dat het een lage bloedsuikerspiegel veroorzaakt.
Wie zou Janumet niet moeten nemen?
Neem Janumet niet in als u:
- diabetes type 1 heeft.
- bepaalde nierproblemen heeft.
- als u metabole acidose of diabetische ketoacidose heeft (verhoogde ketonen in het bloed of urine).
- een allergische reactie heeft gehad op Janumet of sitagliptine (JANUVIA), een van de componenten van Janumet.
- krijgt u een injectie met kleurstof of contrastmiddelen voor een röntgenprocedure, moet Janumet voor een korte tijd worden gestopt. Praat met uw arts over wanneer u moet stoppen met Janumet en wanneer u opnieuw moet beginnen. Zie "Wat is de belangrijkste informatie die ik over Janumet moet weten?"
Wat moet ik mijn arts vertellen vóór en tijdens de behandeling met Janumet?
Janumet is misschien niet geschikt voor u. Vertel uw arts over al uw medische aandoeningen, inclusief als u:
- nierproblemen heeft.
- leverproblemen heeft.
- een allergische reactie heeft gehad op Janumet of sitagliptine (JANUVIA), een van de componenten van Janumet.
- hartproblemen hebben, waaronder congestief hartfalen.
- zijn ouder dan 80 jaar. Patiënten ouder dan 80 jaar mogen Janumet niet gebruiken tenzij hun nierfunctie is gecontroleerd en dit normaal is.
- drink veel alcohol (de hele tijd of op korte termijn "binge" drinken).
- zwanger bent of van plan bent zwanger te worden. Het is niet bekend of Janumet schadelijk is voor uw ongeboren baby. Als u zwanger bent, praat dan met uw arts over de beste manier om uw bloedsuikerspiegel onder controle te houden terwijl u zwanger bent. Als u Janumet tijdens de zwangerschap gebruikt, overleg dan met uw arts over hoe u in het Janumet-register kunt worden opgenomen. Het gratis telefoonnummer voor het zwangerschapsregister is 1-800-986-8999.
- borstvoeding geeft of van plan bent borstvoeding te geven. Het is niet bekend of Janumet in de moedermelk terechtkomt. Praat met uw arts over de beste manier om uw baby te voeden als u Janumet gebruikt.
Vertel uw arts over alle medicijnen die u gebruikt, inclusief recept- en niet-receptplichtige geneesmiddelen, vitamines en kruidensupplementen. Janumet kan de werking van andere geneesmiddelen beïnvloeden en sommige geneesmiddelen kunnen de werking van Janumet beïnvloeden.
Weet welke medicijnen u gebruikt. Houd een lijst van uw geneesmiddelen bij en toon deze aan uw arts en apotheker wanneer u een nieuw geneesmiddel krijgt. Neem contact op met uw arts voordat u met een nieuw geneesmiddel begint.
Hoe moet ik Janumet nemen?
- Uw arts zal u vertellen hoeveel Janumet-tabletten u moet innemen en hoe vaak u deze moet innemen. Neem Janumet precies zoals uw arts u dat heeft verteld.
- Uw arts moet mogelijk uw dosis verhogen om uw bloedsuiker te regelen.
- Uw arts kan Janumet samen met een sulfonylureum (een ander geneesmiddel om de bloedsuikerspiegel te verlagen) voorschrijven. Zie "Wat zijn de mogelijke bijwerkingen van Janumet?" voor informatie over een verhoogd risico op een lage bloedsuikerspiegel.
- Neem Janumet bij de maaltijd om uw kans op maagklachten te verkleinen.
- Blijf Janumet innemen zolang uw arts u dat zegt.
- Als u te veel Janumet inneemt, bel dan onmiddellijk uw arts of gifinformatiecentrum.
- Als u een dosis bent vergeten, neem deze dan in met voedsel zodra u eraan denkt. Als u het zich niet herinnert totdat het tijd is voor uw volgende dosis, sla dan de gemiste dosis over en ga terug naar uw normale schema. Neem niet twee doses Janumet tegelijkertijd in.
- Het kan zijn dat u voor korte tijd moet stoppen met het innemen van Janumet. Bel uw arts voor instructies als u:
- zijn uitgedroogd (hebben te veel lichaamsvocht verloren). Uitdroging kan optreden als u ziek bent met ernstig braken, diarree of koorts, of als u veel minder vocht drinkt dan normaal.
- van plan zijn om een operatie te ondergaan.
- krijgen een injectie met kleurstof of contrastmiddel voor een röntgenprocedure.
Zie "Wat is de belangrijkste informatie die ik over Janumet moet weten?" en "Wie moet Janumet niet nemen?"
- Wanneer uw lichaam onder bepaalde soorten stress staat, zoals koorts, trauma (zoals een auto-ongeluk), infectie of operatie, kan de hoeveelheid diabetesgeneesmiddel die u nodig heeft veranderen. Vertel het uw arts onmiddellijk als u een van deze aandoeningen heeft en volg de instructies van uw arts.
- Controleer uw bloedsuikerspiegel zoals uw arts u dat zegt.
- Blijf uw voorgeschreven dieet en trainingsprogramma volgen terwijl u Janumet gebruikt.
- Praat met uw arts over het voorkomen, herkennen en beheren van een lage bloedsuikerspiegel (hypoglykemie), hoge bloedsuikerspiegel (hyperglykemie) en complicaties van diabetes.
- Uw arts zal uw diabetes controleren met regelmatige bloedtesten, inclusief uw bloedsuikerspiegel en uw hemoglobine A1C.
- Uw arts zal bloedonderzoek doen om uw nierfunctie te controleren vóór en tijdens de behandeling met Janumet.
Wat zijn de mogelijke bijwerkingen van Janumet?
Janumet kan ernstige bijwerkingen veroorzaken. Zie "Wat is de belangrijkste informatie die ik over Janumet moet weten?"
Veel voorkomende bijwerkingen bij het gebruik van Janumet zijn onder meer:
- verstopte of loopneus en keelpijn
- bovenste luchtweginfectie
- diarree
- misselijkheid en overgeven
- gas, maagklachten, indigestie
- zwakheid
- hoofdpijn
Het innemen van Janumet bij de maaltijd kan helpen de veelvoorkomende bijwerkingen van metformine op de maag te verminderen die meestal aan het begin van de behandeling optreden. Neem contact op met uw arts als u ongewone of onverwachte maagproblemen heeft. Maagproblemen die later tijdens de behandeling optreden, kunnen een teken zijn van iets ernstigers.
Bepaalde geneesmiddelen tegen diabetes, zoals sulfonylureumderivaten en meglitiniden, kunnen een lage bloedsuikerspiegel veroorzaken (hypoglykemie). Wanneer Janumet samen met deze geneesmiddelen wordt gebruikt, heeft u mogelijk te lage bloedsuikerspiegel. Uw arts kan lagere doses van het geneesmiddel sulfonylureum of meglitinide voorschrijven. Vertel het uw arts als u problemen heeft met een lage bloedsuikerspiegel.
De volgende aanvullende bijwerkingen zijn bij algemeen gebruik met Janumet of sitagliptine gemeld:
- Ernstige allergische reacties kunnen optreden met Janumet of sitagliptine, een van de geneesmiddelen in Janumet. Symptomen van een ernstige allergische reactie kunnen huiduitslag, netelroos en zwelling van het gezicht, lippen, tong en keel zijn, ademhalingsmoeilijkheden of slikken. Als u een allergische reactie heeft, stop dan met het innemen van Janumet en neem onmiddellijk contact op met uw arts. Uw arts kan een medicijn voorschrijven om uw allergische reactie te behandelen en een ander medicijn voor uw diabetes.
- Verhoogde leverenzymen.
- Ontsteking van de alvleesklier.
Dit zijn niet alle mogelijke bijwerkingen van Janumet. Vraag uw arts om meer informatie.
Vertel het uw arts als u een bijwerking heeft die u stoort, ongebruikelijk is of niet verdwijnt.
Hoe moet ik Janumet bewaren?
Bewaar Janumet bij kamertemperatuur, 68-77 ° F (20-25 ° C).
Houd Janumet en alle geneesmiddelen buiten het bereik van kinderen.
Algemene informatie over het gebruik van Janumet
Geneesmiddelen worden soms voorgeschreven voor aandoeningen die niet worden vermeld in bijsluiters. Gebruik Janumet niet voor een aandoening waarvoor het niet was voorgeschreven. Geef Janumet niet aan andere mensen, zelfs als ze dezelfde symptomen hebben als u. Het kan hen schaden.
Deze folder vat de belangrijkste informatie over Janumet samen. Als u meer informatie wilt, raadpleeg dan uw arts. U kunt uw arts of apotheker om informatie vragen over Janumet die is geschreven voor gezondheidswerkers. Voor meer informatie bel 1-800-622-4477.
Wat zijn de ingrediënten in Janumet?
Actieve ingrediënten: sitagliptine en metforminehydrochloride.
Inactieve ingrediënten: microkristallijne cellulose, polyvinylpyrrolidon, natriumlaurylsulfaat en natriumstearylfumaraat. De filmlaag van de tablet bevat de volgende inactieve ingrediënten: polyvinylalcohol, polyethyleenglycol, talk, titaniumdioxide, rood ijzeroxide en zwart ijzeroxide.
Wat is diabetes type 2?
Type 2 diabetes is een aandoening waarbij uw lichaam onvoldoende insuline aanmaakt en de insuline die uw lichaam aanmaakt, werkt niet zo goed als zou moeten. Je lichaam kan ook teveel suiker maken. Wanneer dit gebeurt, bouwt suiker (glucose) zich op in het bloed. Dit kan leiden tot ernstige medische problemen.
Het belangrijkste doel van de behandeling van diabetes is om uw bloedsuikerspiegel tot een normaal niveau te verlagen. Het verlagen en beheersen van de bloedsuikerspiegel kan complicaties van diabetes, zoals hartproblemen, nierproblemen, blindheid en amputatie helpen voorkomen of vertragen.
Hoge bloedsuikerspiegel kan worden verlaagd door voeding en lichaamsbeweging, en door bepaalde medicijnen indien nodig.
Uitgegeven maart 2009
Gedistribueerd door:
MERCK & CO., INC., Whitehouse Station, NJ 08889, VS.
Laatst bijgewerkt: 03/09
Janumet, Sitagliptin en Metformin Hydrochloride, Patiëntinformatie (In gewoon Engels)
Gedetailleerde informatie over tekenen, symptomen, oorzaken, behandelingen van diabetes
De informatie in deze monografie is niet bedoeld om alle mogelijke toepassingen, aanwijzingen, voorzorgsmaatregelen, interacties tussen geneesmiddelen of bijwerkingen te dekken. Deze informatie is algemeen en is niet bedoeld als specifiek medisch advies. Neem contact op met uw arts, apotheker of verpleegkundige als u vragen heeft over de medicijnen die u gebruikt of meer informatie wilt.
terug naar: Blader door alle medicijnen voor diabetes


