Symlin voor de behandeling van diabetes
Merknaam: Symlin, Symlin Pen
Generieke naam: pramlintide-acetaat
Inhoud:
Beschrijving
farmacologie
Klinische studies
Aanwijzingen en gebruik
Contra
waarschuwingen
Voorzorgsmaatregelen
Bijwerkingen
Overdose
Dosering en administratie
Hoe geleverd
opslagruimte
Symlin, Symlin Pen, pramlintide-acetaat, patiëntinformatie (in gewoon Engels)
WAARSCHUWING
Symlin wordt gebruikt met insuline en is in verband gebracht met een verhoogd risico op door insuline geïnduceerde ernstige hypoglykemie, met name bij patiënten met type 1 diabetes. Wanneer ernstige hypoglykemie geassocieerd met het gebruik van Symlin optreedt, wordt dit gezien binnen 3 uur na een injectie met Symlin. Als ernstige hypoglykemie optreedt tijdens het besturen van een motorvoertuig, zware machines of tijdens andere risicovolle activiteiten, kan ernstig letsel optreden. Juiste patiëntenselectie, zorgvuldige instructie van de patiënt en aanpassing van de insulinedosis zijn cruciale elementen om dit risico te verminderen.
Beschrijving
Symlin® (pramlintide-acetaat) injectie is een antihyperglycemisch geneesmiddel voor gebruik bij patiënten met diabetes die met insuline worden behandeld. Pramlintide is een synthetisch analoog van menselijke amyline, een natuurlijk voorkomend neuro-endocrien hormoon dat wordt gesynthetiseerd door bètacellen van de pancreas en dat bijdraagt aan glucosecontrole tijdens de postprandiale periode. Pramlintide wordt geleverd als een acetaatzout van het synthetische 37-aminozuurpolypeptide, dat in amino verschilt zuursequentie van humaan amylin door vervanging door proline op posities 25 (alanine), 28 (serine) en 29 (Serine).
De structuurformule van pramlintide-acetaat is zoals weergegeven:

Pramlintide-acetaat is een wit poeder met een moleculaire formule van C171H267N51O53S2- x C2H4O2 (3â ‰ ¤xâ ‰ ¤8); het molecuulgewicht is 3949,4. Pramlintide-acetaat is oplosbaar in water.
Symlin is geformuleerd als een heldere, isotone, steriele oplossing voor subcutane (SC) toediening. De wegwerp multidosis SymlinPen® pen-injector bevat 1000 mcg / ml pramlintide (als acetaat); Symlin-injectieflacons bevatten 600 mcg / ml pramlintide (als acetaat). Beide formuleringen bevatten 2,25 mg / ml metacresol als conserveermiddel, D-mannitol als toniciteitsmodificator en azijnzuur en natriumacetaat als pH-modificator. Symlin heeft een pH van ongeveer 4,0.
top
Klinische Farmacologie
Amylin Physiology
Amylin bevindt zich samen met insuline in secretoire korrels en wordt samen met insuline uitgescheiden door bètacellen van de pancreas in reactie op voedselinname. Amylin en insuline vertonen vergelijkbare nuchtere en postprandiale patronen bij gezonde personen (figuur 1).
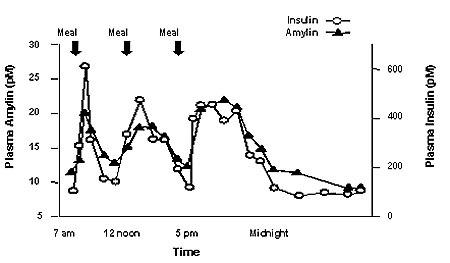
Figuur 1: Secretieprofiel van Amylin en insuline bij gezonde volwassenen
Amylin beïnvloedt de snelheid van postprandiale glucoseverschijnselen via verschillende mechanismen. Amylin vertraagt de maaglediging (d.w.z. de snelheid waarmee voedsel wordt vrijgegeven uit de maag naar de dunne darm) zonder de algehele absorptie van voedingsstoffen te veranderen. Bovendien onderdrukt amyline de glucagonafscheiding (niet genormaliseerd door alleen insuline), wat leidt tot onderdrukking van de endogene glucose-afgifte door de lever. Amylin reguleert ook voedselinname vanwege centraal gemedieerde modulatie van eetlust.
Bij patiënten met insuline die type 2 of type 1 diabetes gebruiken, zijn de bètacellen van de pancreas disfunctioneel of beschadigd, wat resulteert in een verminderde secretie van zowel insuline als amyline als reactie op voedsel.
Werkingsmechanisme
Symlin, door op te treden als een amylinomimeticum, heeft de volgende effecten: 1) modulatie van maaglediging; 2) preventie van de postprandiale stijging van plasmaglucagon; en 3) verzadiging leidend tot verminderde calorie-inname en mogelijk gewichtsverlies.
Maaglediging
De maagledigingssnelheid is een belangrijke determinant van de postprandiale stijging van plasmaglucose. Symlin vertraagt de snelheid waarmee voedsel wordt vrijgegeven uit de maag naar de dunne darm na een maaltijd en dus vermindert het de initiële postprandiale toename van plasmaglucose. Dit effect houdt ongeveer 3 uur aan na toediening van Symlin. Symlin heeft geen invloed op de netto-opname van ingenomen koolhydraten of andere voedingsstoffen.
Postprandiale Glucagon-secretie
Bij patiënten met diabetes zijn glucagonconcentraties abnormaal verhoogd tijdens de postprandiale periode, wat bijdraagt aan hyperglycemie. Van Symlin is aangetoond dat het de postprandiale glucagonconcentraties verlaagt bij insuline-gebruikende patiënten met diabetes.
oververzadiging
Van Symlin toegediend voorafgaand aan een maaltijd is aangetoond dat het de totale calorie-inname vermindert. Dit effect lijkt onafhankelijk te zijn van de misselijkheid die gepaard kan gaan met de behandeling met Symlin.
farmacokinetiek
Absorptie
De absolute biologische beschikbaarheid van een enkele SC-dosis Symlin is ongeveer 30 tot 40%. Subcutane toediening van verschillende doses Symlin in de buik of het bovenbeen van gezonde proefpersonen resulteerde in dosisproportionele maximale plasmaconcentraties (Cmax) en totale blootstelling (uitgedrukt als oppervlakte onder de plasmaconcentratiecurve of (AUC)) (tabel 1).
Tabel 1: Gemiddelde farmacokinetische parameters na toediening van afzonderlijke SC-doses van Symlin
| SC dosis (Mcg) |
AUC (0-β) (Pmol * min / l) |
Cmax (Pmol / L) |
Tmax (Min) |
Eliminatie t ½ (Min) |
|---|---|---|---|---|
| 30 | 3750 | 39 | 21 | 55 |
| 60 | 6778 | 79 | 20 | 49 |
| 90 | 8507 | 102 | 19 | 51 |
| 120 | 11970 | 147 | 21 | 48 |
Injectie van Symlin in de arm toonde hogere blootstelling met grotere variabiliteit, vergeleken met blootstelling na injectie van Symlin in de buik of dijbeen.
Er was geen sterke correlatie tussen de mate van adipositas zoals bepaald door BMI of huidplooidikte metingen en relatieve biologische beschikbaarheid. Injecties toegediend met naalden van 6,0 mm en 12,7 mm leverden een vergelijkbare biologische beschikbaarheid op.
Distributie
Symlin bindt niet uitgebreid aan bloedcellen of albumine (ongeveer 40% van het geneesmiddel is niet gebonden in plasma), en daarom zou de farmacokinetiek van Symlin ongevoelig moeten zijn voor veranderingen in bindingsplaatsen.
Metabolisme en eliminatie
Bij gezonde personen is de halfwaardetijd van Symlin ongeveer 48 minuten. Symlin wordt voornamelijk gemetaboliseerd door de nieren. Des-lys1 pramlintide (2-37 pramlintide), de primaire metaboliet, heeft een vergelijkbare halfwaardetijd en is biologisch actief zowel in vitro als in vivo bij ratten. AUC-waarden zijn relatief constant bij herhaalde dosering, hetgeen wijst op geen bioaccumulatie.
Speciale populaties
Nierinsufficiëntie
Patiënten met matige of ernstige nierinsufficiëntie (ClCr> 20 tot â ‰ ¤50 ml / min) vertoonden geen verhoogde Symlin-blootstelling of verminderde Symlin-klaring vergeleken met personen met een normale nierfunctie. Er zijn geen studies gedaan bij dialysepatiënten.
Leverinsufficiëntie
Er zijn geen farmacokinetische onderzoeken uitgevoerd bij patiënten met leverinsufficiëntie. Op basis van de grote mate van niermetabolisme (zie metabolisme en eliminatie) wordt echter niet verwacht dat leverdysfunctie de bloedconcentraties van Symlin beïnvloedt.
geriatrisch
Er zijn geen farmacokinetische onderzoeken uitgevoerd bij de geriatrische populatie. Symlin mag alleen worden gebruikt bij patiënten waarvan bekend is dat ze de insulineregeling en glucosemonitoring volledig begrijpen en zich eraan houden. Er zijn geen consistente leeftijdgerelateerde verschillen in de activiteit van Symlin waargenomen bij de geriatrische populatie (n = 539 voor patiënten van 65 jaar of ouder in de klinische onderzoeken).
Pediatric
Symlin is niet geëvalueerd bij pediatrische patiënten.
Geslacht
Er is geen onderzoek uitgevoerd om mogelijke gendereffecten op de farmacokinetiek van Symlin te evalueren. Er zijn echter geen consistente geslachtsgerelateerde verschillen in de activiteit van Symlin waargenomen in de klinische onderzoeken (n = 2799 voor mannen en n = 2085 voor vrouwen).
Ras / etniciteit
Er is geen onderzoek uitgevoerd om het effect van etniciteit op de farmacokinetiek van Symlin te evalueren. Er zijn echter geen consistente verschillen in de activiteit van Symlin waargenomen bij patiënten van verschillende aard ras / etniciteit in de klinische proeven (n = 4257 voor wit, n = 229 voor zwart, n = 337 voor Spaans en n = 61 voor andere Etnische afkomst).
Geneesmiddelinteracties
Het effect van Symlin (120 mcg) op de farmacokinetiek van acetaminophen (1000 mg) als marker voor maaglediging werd geëvalueerd bij patiënten met type 2 diabetes (n = 24). Symlin heeft de AUC van paracetamol niet significant gewijzigd. Symlin verminderde echter acetaminophen Cmax (ongeveer 29% met gelijktijdige gelijktijdige toediening) en verhoogde de tijd tot maximale plasmaconcentratie of tmax (variërend van 48 tot 72 minuten) afhankelijk van het tijdstip van toediening van paracetamol ten opzichte van Symlin injectie. Symlin had geen significante invloed op paracetamolmax wanneer acetaminophen 1 tot 2 uur vóór de injectie met Symlin werd toegediend. De tmax van acetaminophen was significant verhoogd wanneer acetaminophen gelijktijdig met of tot 2 uur na de injectie met Symlin werd toegediend (zie VOORZORGSMAATREGELEN, Geneesmiddelinteracties).
farmacodynamiek
In klinische onderzoeken bij patiënten met insuline met type 2 en type 1 diabetes resulteerde de toediening van Symlin in een vermindering van de gemiddelde postprandiale glucoseconcentraties, verminderde glucoseschommelingen en verminderd voedsel inname. De doses Symlin verschillen voor insuline-gebruikende type 2 en type 1 patiënten (zie DOSERING EN ADMINISTRATIE).
Vermindering van postprandiale glucoseconcentraties
Symlin subcutaan toegediend onmiddellijk voorafgaand aan een maaltijd verlaagde de plasmaglucoseconcentraties na de maaltijd bij gebruik met gewone insuline of snelwerkende insuline-analogen (figuur 2). Deze verlaging van postprandiale glucose verminderde de hoeveelheid benodigde kortwerkende insuline en beperkte glucoseschommelingen op basis van 24-uurs glucosemonitoring. Wanneer snelwerkende analoge insulines werden gebruikt, hadden de plasmaglucoseconcentraties de neiging om te stijgen tijdens het interval tussen 150 minuten na de injectie met Symlin en de volgende maaltijd (zie DOSERING EN ADMINISTRATIE).
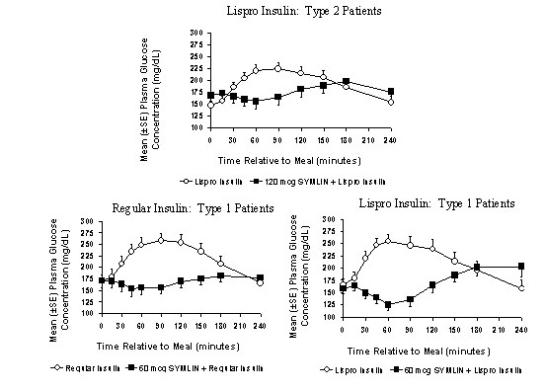
Figuur 2: Postprandiale plasmaglucoseprofielen bij patiënten met diabetes type 2 en type 1 die symlin en / of insuline krijgen
Verminderde voedselinname
Een enkele, subcutane dosis Symlin 120 mcg (type 2) of 30 mcg (type 1) toegediend 1 uur voorafgaand aan een onbeperkte buffetmaaltijd werd geassocieerd met verlagingen van de totale calorie-inname (placebo-afgetrokken gemiddelde veranderingen van respectievelijk ~ 23% en 21%), die plaatsvonden zonder afname van de maaltijd looptijd.
top
Klinische studies
Een totaal van 5325 patiënten en gezonde vrijwilligers ontvingen Symlin in klinische onderzoeken. Dit omvat 1688 met type 2 diabetes en 2375 met type 1 diabetes op korte en lange termijn gecontroleerd klinische proeven, langdurige ongecontroleerde klinische proeven en een open-label onderzoek in de klinische praktijk setting.
Klinische studies bij diabetes type 2
De werkzaamheid van een reeks Symlin-doses werd geëvalueerd in verschillende placebogecontroleerde en open-label klinische onderzoeken bij patiënten die insuline gebruiken met type 2 diabetes. Op basis van de resultaten die in deze studies zijn verkregen, is de aanbevolen dosis Symlin voor patiënten met insuline-gebruikende diabetes type 2 120 mcg, onmiddellijk voorafgaand aan de hoofdmaaltijden toegediend.
Twee langetermijn (26 tot 52 weken), gerandomiseerde, dubbelblinde, placebogecontroleerde onderzoeken met Symlin zijn uitgevoerd bij patiënten met diabetes type 2 met insuline met een vaste dosis om het Symlin-effect te isoleren. Demografische en baseline kenmerken voor de 871 met Symlin behandelde patiënten zijn als volgt: het gemiddelde baseline HbA1c varieerde van 9,0 tot 9,4%, de gemiddelde leeftijd was 56,4 tot 59,1 jaar, de gemiddelde duur van diabetes varieerde van 11,5 tot 14,4 jaar en de gemiddelde BMI varieerde van 30,1 tot 34,4 kg / m2. In beide studies werd Symlin of placebo toegevoegd aan de bestaande diabetestherapieën van de deelnemers, waaronder insuline met of zonder een sulfonylureummiddel en / of metformine.
Tabel 2 geeft een samenvatting van de samengestelde resultaten in beide onderzoeken voor patiënten die na 6 maanden behandeling werden toegewezen aan de dosis van 120 mcg.
Tabel 2: Gemiddelde (SE) verandering in HbA1c, gewicht en insuline na 6 maanden in de dubbelblinde, placebogecontroleerde onderzoeken bij patiënten met insuline-gebruik type 2 diabetes
| veranderlijk | Placebo | Symlin (120 mcg) |
|---|---|---|
| Baseline HbA1c (%) | 9.3 (0.08) | 9.1 (0.06) |
| Verandering in HbA1c na 6 maanden ten opzichte van baseline (%) | −0.17 (0.07) | −0.57 (0.06)* |
| Placebo-afgetrokken HbA1c-verandering na 6 maanden (%) | NA | −0.40 (0.09)* |
| Gewicht basislijn (kg) | 91.3 (1.2) | 92.5 (1.2) |
| Gewichtsverandering na 6 maanden ten opzichte van baseline (kg) | +0.2 (0.2) | −1.5 (0.2)* |
| Placebo-afgetrokken gewichtsverandering na 6 maanden (kg) | NA | −1.7 (0.3)* |
| Procentuele verandering in insulinedoses na 6 maanden: snel / kortwerkend | +6.5 (2.7) | −3.0 (1.6)* |
| Procentuele verandering in insulinedoses na 6 maanden: langwerkend | +5.2 (1.4) | −0.2 (1.3)* |
|
In een cohort van 145 patiënten die twee jaar Symlin-behandeling hadden voltooid, waren de HbA1c- en gewichtsreducties bij aanvang: respectievelijk â respectively’0,40% en −0,36 kg.
Open-label onderzoek in de klinische praktijk
Een open-label studie van Symlin werd uitgevoerd bij de aanbevolen dosis van 120 mcg bij 166 patiënten met insuline-gebruikende diabetes type 2 die met behulp van alleen insuline geen glycemische doelen konden bereiken. Bij deze patiënten werd een flexibel doseringsinsuline toegepast (zie DOSERING EN ADMINISTRATIE). In deze studie hebben patiënten hun insulineregime aangepast op basis van glucosemonitoring vóór en na de maaltijd. Bij aanvang bedroeg de gemiddelde HbA1c 8,3%, de gemiddelde leeftijd was 54,4 jaar, de gemiddelde duur van diabetes was 13,3 jaar en de gemiddelde BMI was 38,6 kg / m2. Symlin kreeg belangrijke maaltijden toegediend. Behandeling met Symlin plus insuline gedurende 6 maanden resulteerde in een baseline-afgetrokken gemiddelde HbA1c-reductie van âˆ'0,56 ± 0,15% en een baseline-afgetrokken gemiddelde gewichtsreductie van −2,76 ± 0,34 kg. Deze veranderingen werden bereikt met reducties in doses van totale, kortwerkende en langwerkende insuline (respectievelijk −6,4 ± 2,66, −10,3 ± 4,84 en −4,20 ± 2,42%).
Klinische studies bij diabetes type 1
De werkzaamheid van een reeks Symlin-doses werd geëvalueerd in verschillende placebogecontroleerde en open-label klinische onderzoeken bij patiënten met diabetes type 1. Op basis van de resultaten die in deze onderzoeken zijn verkregen, is de aanbevolen dosis Symlin voor patiënten met diabetes type 1 30 mcg of 60 mcg, onmiddellijk voorafgaand aan de grote maaltijden toegediend.
Drie langetermijn (26 tot 52 weken), gerandomiseerde, dubbelblinde, placebogecontroleerde onderzoeken met Symlin werden uitgevoerd bij patiënten met type 1 diabetes (N = 1717). Twee van deze onderzoeken lieten slechts minimale aanpassingen van insuline toe om het Symlin-effect te isoleren; in de derde studie werden insuline-aanpassingen gemaakt volgens de standaard medische praktijk. Demografische en baseline kenmerken voor de 1179 met Symlin behandelde patiënten waren als volgt: het gemiddelde HbA1c-bereik bij baseline was 8,7 tot 9,0%, gemiddelde leeftijdscategorie was 37,3 tot 41,9 jaar, gemiddelde duur van diabetesbereik 15,5 tot 19,2 jaar, en gemiddelde BMI-bereik was 25,0 tot 26,8 kg / m2. Symlin of placebo werd toegevoegd aan bestaande insulinetherapieën.
Tabel 3 geeft een samenvatting van de samengestelde resultaten in deze studies voor patiënten toegewezen aan de dosis van 30 of 60 mcg na 6 maanden behandeling.
Tabel 3: Gemiddelde (SE) verandering in HbA1c, gewicht en insuline na 6 maanden in de dubbelblinde, placebogecontroleerde onderzoeken bij patiënten met type 1 diabetes
| veranderlijk | Placebo | Symlin (30 of 60 mcg) |
|---|---|---|
| Baseline HbA1c (%) | 9.0 (0.06) | 8.9 (0.04) |
| Verandering in HbA1c na 6 maanden ten opzichte van baseline (%) | −0.10 (0.05) | −0.43 (0.04)* |
| Placebo-afgetrokken HbA1c-verandering na 6 maanden (%) | NA | −0.33 (0.06)* |
| Gewicht basislijn (kg) | 75.1 (0.6) | 76.1 (0.5) |
| Gewichtsverandering na 6 maanden ten opzichte van baseline (kg) | +0.6 (0.1) | −1.1 (0.1)* |
| Placebo-afgetrokken gewichtsverandering na 6 maanden (kg) | NA | −1.7 (0.1)* |
| Procentuele verandering in insulinedoses na 6 maanden: snel / kortwerkend | +1.7 (3.3) | −3.6 (2.9) |
| Procentuele verandering in insulinedoses na 6 maanden: langwerkend | +2.5 (1.9) | +1.9 (1.3) |
|
* Statistisch significante reductie vergeleken met placebo (p-waarde <0,05). |
In een cohort van 73 patiënten die twee jaar behandeling met Symlin voltooiden, waren de baseline-afgetrokken HbA1c- en gewichtsveranderingen respectievelijk: − 0,35% en 0,60 kg.
Symlin dosis-titratie-onderzoek
Een dosistitratieonderzoek van Symlin is uitgevoerd bij patiënten met type 1 diabetes. Patiënten met een relatief goede glykemische controle bij aanvang (gemiddelde HbA1c = 8,1%) werden gerandomiseerd om insuline plus placebo of insuline plus Symlin te ontvangen. Andere kenmerken bij aanvang en demografie waren: gemiddelde leeftijd van 41 jaar, gemiddelde duur van diabetes van 20 jaar, gemiddelde BMI van 28 kg / m2. Symlin werd gestart met een dosis van 15 mcg en werd met wekelijkse tussenpozen naar boven getitreerd met stappen van 15 mcg tot doses van 30 mcg of 60 mcg, afhankelijk van of patiënten misselijkheid ervoeren. Zodra een getolereerde dosis van 30 mcg of 60 mcg werd bereikt, werd de dosis Symlin gehandhaafd voor de rest van de studie (Symlin werd toegediend vóór de hoofdmaaltijd). Tijdens de titratie van Symlin werd de insulinedosis (meestal de kort / snelwerkende insuline) met 30-50% verlaagd om hypoglykemie te verminderen. Nadat een getolereerde Symlin-dosis was bereikt, werden de insulinedosisaanpassingen uitgevoerd volgens de standaard klinische praktijk, op basis van bloedglucosebewaking vóór en na de maaltijd. Na 6 maanden behandeling vertoonden patiënten behandeld met Symlin en insuline en patiënten behandeld met insuline en placebo een equivalente verlaging van de gemiddelde HbA1c (âˆ'0,47 ± 0,07% vs. −0,49 ± 0,07%, respectievelijk); patiënten op Symlin verloren gewicht (âˆ'1,33 ± 0,31 kg ten opzichte van de uitgangswaarde en −2,6 kg ten opzichte van placebo plus met insuline behandelde patiënten). Met Symlin behandelde patiënten gebruikten minder totale insuline (−11,7% ten opzichte van de uitgangswaarde) en minder korte / snelwerkende insuline (−22,8%) ten opzichte van de uitgangswaarde.
Open-label onderzoek in de klinische praktijk
Een open-label studie van Symlin werd uitgevoerd bij patiënten met diabetes type 1 die met behulp van alleen insuline geen glycemische doelen konden bereiken. Bij deze patiënten werd een flexibel doseringsinsuline toegepast nadat de titratie van Symlin was voltooid (zie DOSERING EN ADMINISTRATIE). In deze studie hebben patiënten hun insulineregime aangepast op basis van glucosemonitoring vóór en na de maaltijd. Bij aanvang was de gemiddelde HbA1c 8,0%, de gemiddelde leeftijd was 42,7 jaar, de gemiddelde duur van diabetes was 21,2 jaar en de gemiddelde BMI was 28,6 kg / m2. De dagelijkse dosering van Symlin was 30 mcg of 60 mcg bij grote maaltijden.
Symlin plus insuline verminderde HbA1c en lichaamsgewicht vanaf de basislijn na 6 maanden met respectievelijk gemiddeld 0,18% en 3,0 kg. Deze veranderingen in glycemische controle en lichaamsgewicht werden bereikt met verminderingen van totale doses, kortwerkende en langwerkende insuline (−12,0 ± 1,36, −21,7 ± 2,81 en −0,4 ± 1,59%, respectievelijk).
top
Aanwijzingen en gebruik
Symlin wordt gegeven tijdens de maaltijd en is geïndiceerd voor:
- Type 1 diabetes, als aanvullende behandeling bij patiënten die maaltijdinsuline-therapie gebruiken en die ondanks optimale insulinetherapie de gewenste glucosecontrole niet hebben bereikt.
- Type 2 diabetes, als aanvullende behandeling bij patiënten die maaltijdinsuline-therapie gebruiken en deze niet hebben bereikt gewenste glucosecontrole ondanks optimale insulinetherapie, met of zonder een gelijktijdig sulfonylureummiddel en / of metformine.
top
Contra
Symlin is gecontra-indiceerd bij patiënten met een van de volgende:
- een bekende overgevoeligheid voor Symlin of een van zijn componenten, inclusief metacresol;
- een bevestigde diagnose van gastroparese;
- hypoglykemie onbewustheid.
top
waarschuwingen
Selectie van patiënten
Een juiste selectie van patiënten is van cruciaal belang voor een veilig en effectief gebruik van Symlin
Voor aanvang van de therapie moeten de HbA1c van de patiënt, recente bloedglucosemonitoringsgegevens, geschiedenis van door insuline geïnduceerde hypoglykemie, huidig insulineregime en lichaamsgewicht worden beoordeeld. Behandeling met Symlin dient alleen te worden overwogen bij patiënten met insuline-gebruik type 2 of type 1 diabetes die aan de volgende criteria voldoen:
- zijn er niet in geslaagd om adequate glykemische controle te bereiken ondanks geïndividualiseerd insulinebeheer;
- krijgen voortdurende zorg onder begeleiding van een zorgverlener die bekwaam is in het gebruik van insuline en ondersteund wordt door de diensten van diabetesopvoeder (s).
Patiënten die aan een van de volgende criteria voldoen, mogen NIET in aanmerking worden genomen voor behandeling met Symlin:
- slechte naleving van het huidige insulineregime;
- slechte naleving van voorgeschreven zelfbloedglucosebewaking;
- een HbA1c> 9% hebben;
- terugkerende ernstige hypoglykemie die gedurende de afgelopen 6 maanden assistentie vereist;
- aanwezigheid van hypoglykemie onbewustheid;
- bevestigde diagnose van gastroparese;
- vereisen het gebruik van geneesmiddelen die gastro-intestinale motiliteit stimuleren;
- pediatrische patiënten.
hypoglykemie
Symlin alleen veroorzaakt geen hypoglykemie. Symlin is echter geïndiceerd voor gelijktijdige toediening met insulinetherapie en in deze instelling Symlin verhoogt het risico op insuline-geïnduceerde ernstige hypoglykemie, vooral bij patiënten met type 1 diabetes. Ernstige hypoglykemie geassocieerd met Symlin treedt op binnen de eerste 3 uur na een injectie met Symlin. Als ernstige hypoglykemie optreedt tijdens het besturen van een motorvoertuig, zware machines of tijdens andere risicovolle activiteiten, kan ernstig letsel optreden. Daarom moeten bij het invoeren van Symlin-therapie passende voorzorgsmaatregelen worden genomen om te voorkomen dat het risico op door insuline geïnduceerde ernstige hypoglykemie wordt verhoogd. Deze voorzorgsmaatregelen omvatten frequente glucosemetingen vóór en na de maaltijd gecombineerd met een initiële vermindering van 50% van de doses voor kortwerkende insuline vóór de maaltijd (zie DOSERING EN ADMINISTRATIE).
Symptomen van hypoglykemie kunnen zijn: honger, hoofdpijn, zweten, tremor, prikkelbaarheid of concentratiestoornissen. Snelle verlagingen van de bloedglucoseconcentraties kunnen dergelijke symptomen veroorzaken, ongeacht de glucosewaarden. Meer ernstige symptomen van hypoglykemie zijn onder meer bewustzijnsverlies, coma of epileptische aanvallen.
Vroege waarschuwingssymptomen van hypoglykemie kunnen verschillend of minder uitgesproken zijn onder bepaalde omstandigheden, zoals langdurige diabetes; diabetische zenuwziekte; gebruik van medicijnen zoals bètablokkers, clonidine, guanethidine of reserpine; of versterkte diabetescontrole.
De toevoeging van een antihyperglycemisch middel zoals Symlin aan een bestaand regime van een of meer antihyperglycemische middelen (bijvoorbeeld insuline, sulfonylureum), of andere middelen die het risico op hypoglykemie kunnen verhogen, kunnen verdere aanpassingen van de insulinedosis en in het bijzonder nauwkeurige controle van bloedglucose noodzakelijk maken.
Hierna volgen voorbeelden van stoffen die het bloedglucoseverlagende effect en de gevoeligheid voor hypoglykemie kunnen vergroten: orale antidiabetica producten, ACE-remmers, diisopyramide, fibraten, fluoxetine, MAO-remmers, pentoxifylline, propoxyfeen, salicylaten en sulfonamide antibiotica.
Klinische studies met een gecontroleerde hypoglycemische uitdaging hebben aangetoond dat Symlin de contra-regulerende hormonale respons op door insuline geïnduceerde hypoglykemie niet verandert. Evenzo was bij met Symlin behandelde patiënten de perceptie van hypoglycemische symptomen niet veranderd bij plasmaglucoseconcentraties van slechts 45 mg / dl.
top
Voorzorgsmaatregelen
Algemeen
Hypoglykemie (zie WAARSCHUWINGEN).
Symlin moet met voorzichtigheid worden voorgeschreven aan personen met een visuele beperking of handigheid.
Informatie voor patiënten
Zorgverleners moeten patiënten informeren over de mogelijke risico's en voordelen van Symlin-therapie. Zorgverleners moeten patiënten ook informeren over zelfmanagementmethoden, waaronder glucosemonitoring, juiste injectietechniek, timing van dosering en juiste opslag van Symlin. Versterk bovendien het belang van naleving van maaltijdplanning, fysieke activiteit, herkenning en behandeling van hypoglykemie en hyperglykemie en beoordeling van diabetescomplicaties. Raadpleeg patiënten voor meer informatie in de Symlin Medicatiehandleiding en de gebruiksaanwijzing van de patiënt.
Instrueer patiënten bij het omgaan met speciale situaties zoals bijkomende omstandigheden (ziekte of stress), een onvoldoende of weggelaten insulinedosis, onbedoelde toediening van verhoogde insuline of Symlin-dosis, onvoldoende inname van voedsel of gemist maaltijden.
Symlin en insuline moeten altijd als afzonderlijke injecties worden toegediend en mogen nooit worden gemengd.
Vrouwen met diabetes moeten het advies krijgen om hun arts te informeren als ze zwanger zijn of zwanger zijn.
Nierinsufficiëntie
De doseringsvereisten voor Symlin zijn niet gewijzigd bij patiënten met matige of ernstige nierinsufficiëntie (ClCr> 20 tot â ‰ ¤50 ml / min). Er zijn geen studies gedaan bij dialysepatiënten (zie KLINISCHE FARMACOLOGIE; Speciale populaties).
Leverinsufficiëntie
Er zijn geen onderzoeken uitgevoerd bij patiënten met leverinsufficiëntie. Er wordt echter niet verwacht dat leverdisfunctie de bloedconcentraties van Symlin beïnvloedt (zie KLINISCHE FARMACOLOGIE; Speciale populaties).
Allergie
Lokale allergie
Patiënten kunnen roodheid, zwelling of jeuk op de injectieplaats ervaren. Deze kleine reacties verdwijnen meestal binnen enkele dagen tot enkele weken. In sommige gevallen kunnen deze reacties verband houden met andere factoren dan Symlin, zoals irriterende stoffen in een huidreinigingsmiddel of een onjuiste injectietechniek.
Systemische allergie
In gecontroleerde klinische onderzoeken tot 12 maanden werden potentiële systemische allergische reacties gemeld bij 65 (5%) van type 2-patiënten en 59 (5%) van type 1 met Symlin behandelde patiënten. Vergelijkbare reacties werden gemeld door respectievelijk 18 (4%) en 28 (5%) van met placebo behandelde type 2 en type 1 patiënten. Geen enkele patiënt die Symlin kreeg, werd uit een onderzoek teruggetrokken vanwege een mogelijke systemische allergische reactie.
Geneesmiddelinteracties
Vanwege de effecten op het legen van de maag, dient Symlin-therapie niet te worden overwogen voor patiënten die geneesmiddelen gebruiken die het maag-darmkanaal veranderen motiliteit (bijvoorbeeld anticholinerge middelen zoals atropine) en middelen die de intestinale absorptie van voedingsstoffen vertragen (bijvoorbeeld Î ± -glucosidase remmers). Patiënten die deze geneesmiddelen gebruiken, zijn niet in klinische onderzoeken onderzocht.
Symlin kan de absorptie van gelijktijdig toegediende orale medicijnen vertragen. Wanneer het snelle begin van een gelijktijdig oraal toegediend middel een kritische bepalende factor voor de effectiviteit is (zoals pijnstillers), moet het middel ten minste 1 uur vóór of 2 uur na Symlin worden toegediend injectie.
In klinische onderzoeken veranderde het gelijktijdig gebruik van sulfonylureumderivaten of biguaniden het bijwerkingenprofiel van Symlin niet. Er zijn geen formele interactiestudies uitgevoerd om het effect van Symlin op de kinetiek van orale antidiabetica te beoordelen.
Symlin en insuline mengen
De farmacokinetische parameters van Symlin werden veranderd wanneer ze onmiddellijk voorafgaand aan injectie werden gemengd met reguliere, NPH en 70/30 voorgemengde formuleringen van recombinant humane insuline. Symlin en insuline mogen daarom niet worden gemengd en moeten afzonderlijk worden toegediend.
Carcinogenese, mutagenese, aantasting van de vruchtbaarheid
carcinogenese
Een tweejarig carcinogeniteitsonderzoek werd uitgevoerd bij CD-1-muizen met doses van 0,2, 0,5 en 1,2 mg / kg / dag Symlin (32, 67 en 159 keer de blootstelling als gevolg van de maximale aanbevolen dosis voor mensen op basis van het gebied onder de plasmaconcentratiecurve of AUC, respectievelijk). Er werden geen door geneesmiddelen geïnduceerde tumoren waargenomen. Een tweejarig carcinogeniteitsonderzoek werd uitgevoerd bij Sprague-Dawley-ratten met doses van 0,04, 0,2 en 0,5 mg / kg / dag van Symlin (3, 9 en 25 keer de blootstelling als gevolg van de maximale aanbevolen dosis voor mensen op basis van AUC, respectievelijk). In geen enkel orgaan werden door geneesmiddelen veroorzaakte tumoren waargenomen.
mutagenese
Symlin was niet mutageen in de Ames-test en verhoogde de chromosomale aberratie in de menselijke lymfocyten-test niet. Symlin was niet clastogeen in de in vivo micronucleustest bij muizen of in de chromosomale afwijkingstest met ovariumcellen van de Chinese hamster.
Aantasting van de vruchtbaarheid
Toediening van 0,3, 1 of 3 mg / kg / dag Symlin (8, 17 en 82 keer de blootstelling als gevolg van de maximale aanbevolen dosis voor mensen op basis van lichaamsoppervlak) hadden geen significante effecten op de vruchtbaarheid bij mannen of vrouwen ratten. De hoogste dosis van 3 mg / kg / dag resulteerde in dystocie bij 8/12 vrouwelijke ratten secundair aan significante verlagingen van serumcalciumspiegels.
Zwangerschap
Teratogene effecten: Zwangerschap Categorie C
Er zijn geen adequate en goed gecontroleerde studies uitgevoerd bij zwangere vrouwen. Studies in geperfuseerde humane placenta geven aan dat Symlin een laag potentieel heeft om de moeder / foetale placentabarrière te passeren. Embryofetale toxiciteitsstudies met Symlin zijn uitgevoerd bij ratten en konijnen. Verhogingen van aangeboren afwijkingen (neuraal buisdefect, gespleten gehemelte, exencefalie) werden waargenomen bij foetussen van ratten die werden behandeld tijdens organogenese met 0,3 en 1,0 mg / kg / dag (10 en 47 keer de blootstelling als gevolg van de maximale aanbevolen dosis voor mensen op basis van AUC, respectievelijk). Toediening van doses tot 0,3 mg / kg / dag Symlin (9 maal de maximale aanbevolen dosis op basis van AUC) aan zwangere konijnen had geen nadelige effecten op de ontwikkeling van het embryofoetaal; reproductiestudies bij dieren zijn echter niet altijd voorspellend voor de menselijke respons. Symlin mag alleen tijdens de zwangerschap worden gebruikt als door de arts is vastgesteld dat het potentiële voordeel het potentiële risico voor de foetus rechtvaardigt.
Moeders die borstvoeding geven
Het is onbekend of Symlin wordt uitgescheiden in moedermelk. Veel geneesmiddelen, waaronder peptiden, worden uitgescheiden in moedermelk. Daarom moet Symlin alleen worden toegediend aan vrouwen die borstvoeding geven als door de arts is vastgesteld dat het potentiële voordeel opweegt tegen het potentiële risico voor de baby.
Gebruik bij kinderen
De veiligheid en effectiviteit van Symlin bij pediatrische patiënten zijn niet vastgesteld.
Geriatrisch gebruik
Symlin is onderzocht bij patiënten in de leeftijd van 15 tot 84 jaar oud, waaronder 539 patiënten van 65 jaar of ouder. De verandering in HbA1c-waarden en hypoglykemiefrequenties verschilde niet per leeftijd, maar een grotere gevoeligheid bij sommige oudere personen kan niet worden uitgesloten. Daarom moeten zowel Symlin- als insulineregimes zorgvuldig worden beheerd om een verhoogd risico op ernstige hypoglykemie te voorkomen.
top
Bijwerkingen
Bijwerkingen (met uitzondering van hypoglykemie, hieronder besproken) vaak geassocieerd met Symlin bij gelijktijdige toediening met een vaste dosis insuline in de langetermijn, placebo-gecontroleerde onderzoeken bij patiënten die insuline gebruiken type 2 en type 1 patiënten worden gepresenteerd in tabel 4 en tabel 5, respectievelijk. Dezelfde bijwerkingen werden ook aangetoond in de open-label klinische praktijkstudie, waarbij flexibele insulinedosering werd toegepast.
Tabel 4: Door de behandeling optredende bijwerkingen die optreden met â ‰ ¥ 5% incidentie en grotere incidentie met Symlin vergeleken met Placebo in langetermijn, placebogecontroleerde onderzoeken. Incidentie van dezelfde gebeurtenissen in de open-label klinische praktijkstudie (patiënten met insuline-gebruik type 2 diabetes, 120 mcg)
| Lange termijn, placebogecontroleerde onderzoeken | Open-label, klinische praktijkstudie | ||
|---|---|---|---|
| Placebo + insuline (N (%)) (N = 284) |
Symlin + insuline (N (%)) (N = 292) |
Symlin + insuline (N (%)) (N = 166) |
|
| Misselijkheid | 34 (12) | 81 (28) | 53 (30) |
| Hoofdpijn | 19 (7) | 39 (13) | 8 (5) |
| anorexia | 5 (2) | 27 (9) | 1 (<1) |
| braken | 12 (4) | 24 (8) | 13 (7) |
| Buikpijn | 19 (7) | 23 (8) | 3 (2) |
| Vermoeidheid | 11 (4) | 20 (7) | 5 (3) |
| Duizeligheid | 11 (4) | 17 (6) | 3 (2) |
| hoesten | 12 (4) | 18 (6) | 4 (2) |
| keelholteontsteking | 7 (2) | 15 (5) | 6 (3) |
Tabel 5: Behandeling-Opkomende bijwerkingen die optreden met â ‰ ¥ 5% incidentie en grotere incidentie met Symlin in vergelijking met Placebo in langetermijn, placebogecontroleerde onderzoeken. Incidentie van dezelfde gebeurtenissen in de open-label klinische praktijkstudie (patiënten met type 1 diabetes, 30 of 60 mcg)
| Lange termijn, placebogecontroleerde onderzoeken | Open-label, klinische praktijkstudie | ||
|---|---|---|---|
| Placebo + insuline (n (%)) (N = 538) |
Symlin + insuline (n (%)) (N = 716) |
Symlin + insuline (n (%)) (N = 265) |
|
| Misselijkheid | 92 (17) | 342 (48) | 98 (37) |
| anorexia | 12 (2) | 122 (17) | 0 (0) |
| Schade toegebracht | 55 (10) | 97 (14) | 20 (8) |
| braken | 36 (7) | 82 (11) | 18 (7) |
| arthralgie | 27 (5) | 51 (7) | 6 (2) |
| Vermoeidheid | 22 (4) | 51 (7) | 12 (4.5) |
| Allergische reactie | 28 (5) | 41 (6) | 1 (<1) |
| Duizeligheid | 21 (4) | 34 (5) | 5 (2) |
De meeste bijwerkingen waren van gastro-intestinale aard. Bij patiënten met type 2 of type 1 diabetes was de incidentie van misselijkheid aan het begin van de behandeling met Symlin hoger en nam met de tijd af bij de meeste patiënten. De incidentie en ernst van misselijkheid worden verminderd wanneer Symlin geleidelijk wordt getitreerd tot de aanbevolen doses (zie DOSERING EN ADMINISTRATIE).
Ernstige hypoglykemie
Symlin alleen (zonder de gelijktijdige toediening van insuline) veroorzaakt geen hypoglykemie. Symlin is echter geïndiceerd als een aanvullende behandeling bij patiënten die maaltijdinsuline-therapie en gelijktijdige toediening gebruiken Symlin met insuline kan het risico op insuline-geïnduceerde hypoglykemie verhogen, vooral bij patiënten met diabetes type 1 (zien Boxed Waarschuwing). De incidentie van ernstige hypoglykemie tijdens het klinische ontwikkelingsprogramma van Symlin is samengevat in tabel 6 en tabel 7.
Tabel 6: Incidentie en voorvalfrequentie van ernstige hypoglykemie bij langdurige, placebogecontroleerde en open-label, klinische praktijkstudies bij patiënten met insuline-gebruik type 2 diabetes
| Langetermijn, Placebo-gecontroleerde studies (Geen insulinedosisreductie tijdens initiatie) |
Open-label, Klinische praktijkstudie (Insulinedosisreductie tijdens initiatie) |
|||||
|---|---|---|---|---|---|---|
| Placebo + insuline | Symlin + insuline | Symlin + insuline | ||||
|
Ernstige hypoglykemie |
0-3 Maanden (N = 284) |
>3-6 Maanden (N = 251) |
0-3 Maanden (N = 292) |
>3-6 Maanden (N = 255) |
0-3 Maanden (N = 166) |
>3-6 Maanden (N = 150) |
| Patient Vastgestelde * | ||||||
| Event Rate (event rate / patiëntjaar) | 0.24 | 0.13 | 0.45 | 0.39 | 0.05 | 0.03 |
| Incidentie (%) | 2.1 | 2.4 | 8.2 | 4.7 | 0.6 | 0.7 |
| Medisch geassisteerdâ € | ||||||
| Event Rate (event rate / patiëntjaar) | 0.06 | 0.07 | 0.09 | 0.02 | 0.05 | 0.03 |
| Incidentie (%) | 0.7 | 1.2 | 1.7 | 0.4 | 0.6 | 0.7 |
|
* Door patiënt geconstateerde ernstige hypoglykemie: hulp van een ander individu nodig (inclusief hulp bij inname van orale koolhydraten); en / of waarbij toediening van glucagoninjectie, intraveneuze glucose of andere medische interventie vereist is. â € Medisch ondersteunde ernstige hypoglykemie: vereist glucagon, IV glucose, ziekenhuisopname, paramedische assistentie, eerste hulp bezoek en / of beoordeeld als een SAE door de onderzoeker. |
Tabel 7: Incidentie en voorvalpercentage van ernstige hypoglykemie bij langdurige, placebogecontroleerde en open-label, klinische praktijkstudies bij patiënten met type 1 diabetes
| Langetermijn, Placebo-gecontroleerde studies (Geen insulinedosisreductie tijdens initiatie) |
Open-label, Klinische praktijkstudie (Insulinedosisreductie tijdens initiatie) |
|||||
|---|---|---|---|---|---|---|
| Placebo + insuline | Symlin + insuline | Symlin + insuline | ||||
|
Ernstige hypoglykemie |
0-3 Maanden (N = 538) |
>3-6 Maanden (N = 470) |
0-3 Maanden (N = 716) |
>3-6 Maanden (N = 576) |
0-3 Maanden (N = 265) |
>3-6 Maanden (N = 213) |
| Patient Vastgestelde * | ||||||
| Event Rate (event rate / patiëntjaar) | 1.33 | 1.06 | 1.55 | 0.82 | 0.29 | 0.16 |
| Incidentie (%) | 10.8 | 8.7 | 16.8 | 11.1 | 5.7 | 3.8 |
| Medisch geassisteerdâ € | ||||||
| Event Rate (event rate / patiëntjaar) | 0.19 | 0.24 | 0.50 | 0.27 | 0.10 | 0.04 |
| Incidentie (%) | 3.3 | 4.3 | 7.3 | 5.2 | 2.3 | 0.9 |
|
* Door patiënt geconstateerde ernstige hypoglykemie: hulp van een ander individu nodig (inclusief hulp bij inname van orale koolhydraten); en / of waarbij toediening van glucagoninjectie, intraveneuze glucose of andere medische interventie vereist is. â € Medisch ondersteunde ernstige hypoglykemie: vereist glucagon, IV glucose, ziekenhuisopname, paramedische assistentie, eerste hulp bezoek en / of beoordeeld als een SAE door de onderzoeker. |
Postmarketingervaring
Sinds de introductie van Symlin op de markt zijn de volgende bijwerkingen gemeld. Omdat deze gebeurtenissen vrijwillig worden gemeld door een populatie van onzekere omvang, is het niet altijd mogelijk om hun frequentie betrouwbaar te schatten of een oorzakelijk verband met blootstelling aan geneesmiddelen vast te stellen.
Algemeen: reacties op de injectieplaats.
Overdose
Enkelvoudige doses van 10 mg Symlin (83 maal de maximale dosis van 120 mcg) werden toegediend aan drie gezonde vrijwilligers. Ernstige misselijkheid werd gemeld bij alle drie personen en ging gepaard met braken, diarree, vasodilatatie en duizeligheid. Er werd geen hypoglykemie gemeld. Symlin heeft een korte halfwaardetijd en in het geval van overdosering zijn ondersteunende maatregelen aangewezen.
top
Dosering en administratie
De dosering van Symlin verschilt afhankelijk van of de patiënt diabetes type 2 of type 1 heeft (zie hieronder). Bij het starten van de therapie met Symlin is initiële verlaging van de insulinedosis vereist bij alle patiënten (zowel type 2 als type 1) om het risico op insuline-geïnduceerde hypoglykemie te verminderen. Aangezien deze vermindering van insuline kan leiden tot glucoseverhogingen, moeten patiënten regelmatig worden gecontroleerd tot beoordeel Symlin-verdraagbaarheid en het effect op bloedglucose, zodat geïndividualiseerde insuline-aanpassingen kunnen zijn geïnitieerd. Als de therapie met Symlin om welke reden dan ook wordt stopgezet (bijvoorbeeld een operatie of ziekte), moet hetzelfde startprotocol worden gevolgd wanneer de therapie met Symlin opnieuw wordt ingesteld (zie hieronder).
Initiatie van Symlin-therapie
Patiënten met insuline-gebruik type 2 diabetes
Bij patiënten met insuline die diabetes type 2 gebruikt, moet Symlin worden gestart met een dosis van 60 mcg en worden verhoogd tot een dosis van 120 mcg zoals getolereerd.
Patiënten moeten worden geïnstrueerd om:
- Start Symlin subcutaan op 60 mcg, onmiddellijk voorafgaand aan grote maaltijden;
- Vermindering van preprandiale, snelwerkende of kortwerkende insulinedoseringen, inclusief insulines met een vaste mix (70/30) met 50%;
- Bloedglucose regelmatig controleren, inclusief voor en na de maaltijd en voor het slapengaan;
- Verhoog de dosis Symlin tot 120 mcg wanneer er gedurende 3-7 dagen geen klinisch significante misselijkheid is opgetreden. De dosisaanpassingen van Symlin mogen alleen worden uitgevoerd zoals voorgeschreven door de arts. Als de misselijkheid aanhoudt bij de dosis van 120 mcg, moet de dosis Symlin worden verlaagd tot 60 mcg;
- Pas de insulinedoses aan om de glykemische controle te optimaliseren zodra de beoogde dosis Symlin is bereikt en de misselijkheid (indien ervaren) is verdwenen. Insulinedosisaanpassingen mogen alleen worden uitgevoerd zoals voorgeschreven door de arts;
- Neem contact op met een arts die bekwaam is in het gebruik van insuline om ten minste de dosisaanpassingen van Symlin en insuline te bekijken eenmaal per week totdat een beoogde dosis Symlin wordt bereikt, wordt Symlin goed verdragen en zijn de bloedglucoseconcentraties dat stal.
Patiënten met diabetes type 1
Bij patiënten met diabetes type 1 moet Symlin worden gestart met een dosis van 15 mcg en worden getitreerd in stappen van 15 mcg tot een onderhoudsdosis van 30 mcg of 60 mcg zoals getolereerd.
Patiënten moeten worden geïnstrueerd om:
- Start Symlin met een startdosis van 15 mcg subcutaan, onmiddellijk voorafgaand aan grote maaltijden;
- Vermindering van preprandiale, snelwerkende of kortwerkende insulinedoseringen, inclusief insulines met een vaste mix (bijvoorbeeld 70/30) met 50%;
- Bloedglucose regelmatig controleren, inclusief voor en na de maaltijd en voor het slapengaan;
- Verhoog de dosis Symlin naar de volgende stap (30 mcg, 45 mcg of 60 mcg) wanneer er gedurende ten minste 3 dagen geen klinisch significante misselijkheid is opgetreden. De dosisaanpassingen van Symlin mogen alleen worden uitgevoerd zoals voorgeschreven door de arts. Als de misselijkheid op het dosisniveau van 45 of 60 mcg aanhoudt, moet de dosis Symlin worden verlaagd tot 30 mcg. Als de dosis van 30 mcg niet wordt verdragen, moet stopzetting van de behandeling met Symlin worden overwogen;
- Pas de insulinedoses aan om de glykemische controle te optimaliseren zodra de beoogde dosis Symlin is bereikt en de misselijkheid (indien ervaren) is verdwenen. Insulinedosisaanpassingen mogen alleen worden uitgevoerd zoals voorgeschreven door de arts;
- Neem contact op met een arts die bekwaam is in het gebruik van insuline om ten minste de dosisaanpassingen van Symlin en insuline te bekijken eenmaal per week totdat een beoogde dosis Symlin wordt bereikt, wordt Symlin goed verdragen en zijn de bloedglucoseconcentraties dat stal.
Zodra de doeldosis van Symlin is bereikt bij type 2 of type 1 patiënten
Nadat een onderhoudsdosis Symlin is bereikt, moeten zowel insuline-gebruikende patiënten met diabetes type 2 als patiënten met diabetes type 1 worden geïnstrueerd om:
- Pas de insulinedoses aan om de glykemische controle te optimaliseren zodra de beoogde dosis Symlin is bereikt en de misselijkheid (indien ervaren) is verdwenen. Insulinedosisaanpassingen mogen alleen worden uitgevoerd op voorschrift van een arts;
- Neem contact op met een arts in het geval van terugkerende misselijkheid of hypoglykemie. Een verhoogde frequentie van milde tot matige hypoglykemie moet worden gezien als een waarschuwing voor een verhoogd risico op ernstige hypoglykemie.
Toediening
Symlin moet subcutaan worden toegediend onmiddellijk voorafgaand aan elke grote maaltijd (â ‰ ¥ 250 kcal of met â ‰ ¥ 30 g koolhydraten).
Symlin moet vóór injectie op kamertemperatuur zijn om mogelijke reacties op de injectieplaats te verminderen. Elke dosis Symlin moet subcutaan in de buik of dij worden toegediend (toediening in de arm wordt niet aanbevolen vanwege variabele absorptie). Injectieplaatsen moeten zo worden gedraaid dat dezelfde plaats niet herhaaldelijk wordt gebruikt. De gekozen injectieplaats moet ook verschillen van de gekozen locatie voor gelijktijdige insuline-injectie.
- Symlin en insuline moeten altijd als afzonderlijke injecties worden toegediend.
- Symlin mag niet worden gemengd met enig type insuline.
- Als een dosis Symlin wordt gemist, wacht dan tot de volgende geplande dosis en dien de gebruikelijke hoeveelheid toe.
SymlinPen® pen-injector
De SymlinPen® pen-injector is beschikbaar in twee presentaties:
- SymlinPen® 60 pen-injector voor doses van 15 mcg, 30 mcg, 45 mcg, 60 mcg.
- SymlinPen® 120 pen-injector voor doses van 60 mcg en 120 mcg.
Zie de bijbehorende gebruiksaanwijzing voor de patiënt voor instructies voor het gebruik van de SymlinPen® pen-injector.
De patiënt moet worden geadviseerd:
- om te bevestigen dat ze de juiste pen-injector gebruiken die hun voorgeschreven dosis zal leveren;
- bij correct gebruik van de pen-injector, benadrukkend hoe en wanneer een nieuwe pen-injector moet worden opgezet;
- Symlin niet overbrengen van de pen-injector naar een spuit. Dit kan leiden tot een hogere dosis dan bedoeld, omdat Symlin in de pen-injector een hogere concentratie heeft dan Symlin in de Symlin-injectieflacon;
- om de pen-injector en naalden niet met anderen te delen;
- dat naalden niet bij de pen-injector zijn inbegrepen en apart moeten worden gekocht;
- welke naaldlengte en -maat moeten worden gebruikt;
- om voor elke injectie een nieuwe naald te gebruiken.
Symlin-flesjes
Gebruik een U-100 insulinespuit (bij voorkeur 0,3 ml [0,3 cc]) om Symlin uit flacons toe te dienen voor optimale nauwkeurigheid. Als u een spuit gebruikt die is gekalibreerd voor gebruik met U-100-insuline, gebruik dan de onderstaande tabel (tabel 8) om de microgramdosis in stappen van een eenheid te meten.
Tabel 8: Conversie van Symlin-dosis naar equivalenten van insuline-eenheden
| Voorgeschreven dosering (mcg) | Toename met een U-100-spuit (eenheden) | Volume (cc of ml) |
|---|---|---|
| 15 | 2 ½ | 0.025 |
| 30 | 5 | 0.05 |
| 45 | 7 ½ | 0.075 |
| 60 | 10 | 0.1 |
| 120 | 20 | 0.2 |
Gebruik altijd afzonderlijke, nieuwe spuiten en naalden om Symlin- en insuline-injecties te geven.
Stopzetting van de therapie
De behandeling met Symlin moet worden gestaakt als een van de volgende situaties optreedt:
* Terugkerende onverklaarbare hypoglykemie die medische hulp vereist;
* Aanhoudende klinisch significante misselijkheid;
* Niet-naleving van zelfcontrole van bloedglucoseconcentraties;
* Niet-naleving van aanpassingen van de insulinedosis;
* Niet-naleving van geplande contacten met professionele zorgverleners of aanbevolen kliniekbezoeken.
Voorbereiding en behandeling
Symlin moet vóór toediening visueel worden geïnspecteerd op deeltjes of verkleuring wanneer de oplossing en de verpakking dit toelaten.
top
Hoe geleverd
Symlin wordt geleverd als een steriele injectie in de volgende doseringsvormen:
- 1,5 ml wegwerp multidosis SymlinPen® 60 pen-injector met 1000 mcg / ml pramlintide (als acetaat).
- 2,7 ml wegwerp multidosis SymlinPen® 120 pen-injector met 1000 mcg / ml pramlintide (als acetaat).
- Injectieflacon van 5 ml, met 600 mcg / ml pramlintide (als acetaat), voor gebruik met een insulinespuit.
Gebruik een U-100 insulinespuit (bij voorkeur een 0,3 ml [0,3 cc]) om Symlin uit flacons toe te dienen. Als u een spuit gebruikt die is gekalibreerd voor gebruik met U-100 insuline, gebruik dan de grafiek (tabel 8) in de DOSERING EN ADMINISTRATIE sectie om de microgramdosering te meten in eenheden.
Meng Symlin niet met insuline.
Symlin Injection is beschikbaar in de volgende verpakkingsgroottes:
- SymlinPen® 60 pen-injector, met 1000 mcg / ml pramlintide (als acetaat)
2 x 1,5 ml wegwerp multidosis pen-injector
(NDC 66780-115-02) - SymlinPen® 120 pen-injector, met 1000 mcg / ml pramlintide (als acetaat)
2 x 2,7 ml wegwerp multidosis pen-injector
(NDC 66780-121-02) - Injectieflacon van 5 ml, met 600 mcg / ml pramlintide (als acetaat), voor gebruik met een insulinespuit
(NDC 66780-110-01)
opslagruimte
Symlin pen-injectoren en injectieflacons niet in gebruik: Koel (36 ° F tot 46 ° F; 2 ° C tot 8 ° C), en bescherm tegen licht. Niet bevriezen. Niet gebruiken als het product bevroren is geweest. Ongebruikte Symlin (geopend of ongeopend) mag niet worden gebruikt na de vervaldatum (EXP) die staat vermeld op de doos en het etiket.
Symlin pen-injectoren en injectieflacons in gebruik: Na het eerste gebruik 30 dagen in de koelkast bewaren of op een temperatuur van maximaal 30 ° C (86 ° F) bewaren. Gebruik binnen 30 dagen, al dan niet gekoeld.
Opslagomstandigheden zijn samengevat in tabel 9.
Tabel 9: Opslagcondities
| Doseringsvorm | Ongeopend (niet in gebruik) gekoelde |
Open (in gebruik) Gekoeld of temperatuur Tot 86 ° F (30 ° C) |
|---|---|---|
| 1,5 ml pen-injector 2,7 ml pen-injector Injectieflacon van 5 ml |
Tot de vervaldatum | Gebruik binnen 30 dagen |
De SymlinPen® pen-injectors en Symlin-injectieflacons zijn vervaardigd voor: Amylin Pharmaceuticals, Inc. San Diego, CA 92121 VS 1-800-349-8919 http://www.Symlin.com
Alleen Rx
Het Symlin-merk, Symlin-ontwerpmerk en SymlinPen zijn gedeponeerde handelsmerken van Amylin Pharmaceuticals, Inc. Copyright © 2005-2008, Amylin Pharmaceuticals, Inc. Alle rechten voorbehouden.
Laatst bijgewerkt: juli 2008
Symlin, Symlin Pen, pramlintide-acetaat, patiëntinformatie (in gewoon Engels)
De informatie in deze monografie is niet bedoeld om alle mogelijke toepassingen, aanwijzingen, voorzorgsmaatregelen, interacties tussen geneesmiddelen of bijwerkingen te dekken. Deze informatie is algemeen en is niet bedoeld als specifiek medisch advies. Neem contact op met uw arts, apotheker of verpleegkundige als u vragen heeft over de medicijnen die u gebruikt of meer informatie wilt.
terug naar: Blader door alle medicijnen voor diabetes



